Fortyndet vs. koncentreret saltsyre:Vigtigste forskelle forklaret
Fortyndet saltsyre
* Vandkoncentration: En stor mængde vand (opløsningsmiddel) er til stede.
* HCl-koncentration: En lille mængde HCl (opløst stof) opløses i vandet.
* Styrke: Anses for svag. Det har en lavere koncentration af H+ ioner, som er ansvarlige for surhedsgraden.
* Udseende: Ofte gennemsigtig og farveløs (afhængig af urenheder).
* Reaktivitet: Reagerer langsommere og mindre kraftigt end koncentreret syre.
* Sikkerhed: Generelt sikrere at håndtere, men kræver stadig forsigtighed, da det er ætsende.
Koncentreret saltsyre
* Vandkoncentration: En lille mængde vand (opløsningsmiddel) er til stede.
* HCl-koncentration: En stor mængde HCl (opløst stof) er opløst i vandet.
* Styrke: Anses for stærk. Den har en høj koncentration af H+ ioner, hvilket fører til høj surhedsgrad.
* Udseende: Kan have et gulligt skær på grund af opløste urenheder.
* Reaktivitet: Reagerer hurtigt og kraftigt, hvilket potentielt forårsager farlige reaktioner.
* Sikkerhed: Ekstremt farlig og kræver specialiserede håndteringsteknikker og beskyttelsesudstyr.
Nøglepunkter at huske:
* Koncentration betyder noget: Forskellen mellem fortyndet og koncentreret syre koger ned til de relative mængder af vand og syre til stede.
* Surhed og H+ ioner: Koncentrationen af H+ ioner bestemmer direkte syrens styrke (surhed).
* Sikkerhedsforanstaltninger: Håndter altid syrer med ekstrem forsigtighed, især koncentrerede syrer. Brug korrekt sikkerhedsudstyr og følg laboratoriets sikkerhedsretningslinjer.
Eksempler:
* Fortyndet HCl bruges ofte i mavesyreantacida.
* Koncentreret HCl bruges i industrielle processer som metalrensning og produktion af gødning.
Sidste artikelSaltsyre (HCl):Symbol, Fortynding og Repræsentation
Næste artikelZink- og svovlsyrereaktion:Forståelse af den kemiske proces
 Varme artikler
Varme artikler
-
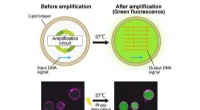 Ny kapacitet til DNA -forstærkning giver løfte om bekæmpelse af sygdommeDNA -amplifikationsproces i kunstige celler. Kredit:Yusuke Sato, Tokyo Institute of Technology DNA -amplifikation - en molekylær fotokopiering teknik, hvor genetisk materiale replikeres - har mang
Ny kapacitet til DNA -forstærkning giver løfte om bekæmpelse af sygdommeDNA -amplifikationsproces i kunstige celler. Kredit:Yusuke Sato, Tokyo Institute of Technology DNA -amplifikation - en molekylær fotokopiering teknik, hvor genetisk materiale replikeres - har mang -
 Hvorfor is har en lavere varmekapacitet end flydende vand - Videnskaben bag klimamoderationAf Kari Wolfe | Opdateret 24. marts 2022 Comstock/Stockbyte/Getty Images At forstå den subtile forskel mellem varmekapaciteten af is og flydende vand er afgørende for at forklare, hvorfor Jordens
Hvorfor is har en lavere varmekapacitet end flydende vand - Videnskaben bag klimamoderationAf Kari Wolfe | Opdateret 24. marts 2022 Comstock/Stockbyte/Getty Images At forstå den subtile forskel mellem varmekapaciteten af is og flydende vand er afgørende for at forklare, hvorfor Jordens -
 Mere bæredygtige mørtler og beton med optimal termisk og mekanisk effektivitetEt fundament bygget i skala for at studere geotermisk energi. Kredit:UPV/EHU Forbruget af råvarer er steget især i industrien generelt, og især i byggeindustrien, midt i voksende bekymring over bæ
Mere bæredygtige mørtler og beton med optimal termisk og mekanisk effektivitetEt fundament bygget i skala for at studere geotermisk energi. Kredit:UPV/EHU Forbruget af råvarer er steget især i industrien generelt, og især i byggeindustrien, midt i voksende bekymring over bæ -
 Forskere forudser nye superhårde materialerKredit:Pixabay/CC0 Public Domain En gruppe Skoltech -forskere brugte machine learning (ML) metoder til at forudsige superhårde materialer baseret på deres krystalstruktur. Forskningen blev offent
Forskere forudser nye superhårde materialerKredit:Pixabay/CC0 Public Domain En gruppe Skoltech -forskere brugte machine learning (ML) metoder til at forudsige superhårde materialer baseret på deres krystalstruktur. Forskningen blev offent
- Hvilke af jordens lag ville være det mindst tætte?
- Hvilken bevægelseslov er det, når du føler en kraft mod den eneste din fod, når du tager skridt …
- Hvilke luftmasser forårsager kolde bølger over det centrale og østlige USA?
- Er der en fuldmåne hver 28. dag?
- Zinkchlorid plus hydrogensulfid danner hvad?
- Hvilken retning kredser Jupiter?


