Zink- og svovlsyrereaktion:Forståelse af den kemiske proces
Reaktionen
Zink (Zn) reagerer med fortyndet svovlsyre (H2SO4) for at producere zinksulfat (ZnSO4) og hydrogengas (H2). Dette er en enkelt forskydningsreaktion.
Kemisk ligning:
Zn(s) + H2SO4(aq) → ZnSO4(aq) + H2(g)
Forklaring:
1. Zinks reaktivitet: Zink er mere reaktivt end brint. Det betyder, at zink kan fortrænge brint fra sin forbindelse, svovlsyre.
2. Reaktionen: Når zink kommer i kontakt med fortyndet svovlsyre, sker følgende:
- Zinkatomerne mister elektroner (oxidation) og bliver til zinkioner (Zn²⁺).
- Hydrogenioner (H⁺) fra syren får elektroner (reduktion) og bliver til brintgas (H₂).
3. Danning af zinksulfat: Zinkionerne (Zn²⁺) kombineres med sulfationer (SO₄²⁻) fra syren og danner zinksulfat (ZnSO4), som opløses i opløsningen.
4. Brandgasudvikling: Den producerede brintgas ses som bobler, der stiger til overfladen af opløsningen.
Observationer:
* Bubbling: Du vil observere kraftig bobling, når brintgas frigives.
* Farveændring: Opløsningen kan blive let uklar, når zinksulfat opløses.
* Varmegenerering: Reaktionen er eksoterm, hvilket betyder, at den frigiver varme, og du vil muligvis bemærke en lille temperaturstigning i opløsningen.
Vigtig bemærkning: Den mosklædte zink er med til at øge overfladearealet af zinken i kontakt med syren, hvilket fremskynder reaktionshastigheden.
Sig til, hvis du har flere spørgsmål!
Sidste artikelFortyndet vs. koncentreret saltsyre:Vigtigste forskelle forklaret
Næste artikelAluminium og saltsyrereaktion:kemi forklaret
 Varme artikler
Varme artikler
-
 En første af sin slags katalysator efterligner naturlige processer til at nedbryde plast og produce…Kredit:Unsplash/CC0 Public Domain Mens genbrug af plast ikke er ny videnskab, nuværende processer gør det ikke økonomisk umagen værd - plastaffald bliver down-cycled til lavere kvalitet, mindre br
En første af sin slags katalysator efterligner naturlige processer til at nedbryde plast og produce…Kredit:Unsplash/CC0 Public Domain Mens genbrug af plast ikke er ny videnskab, nuværende processer gør det ikke økonomisk umagen værd - plastaffald bliver down-cycled til lavere kvalitet, mindre br -
 Verifikation af whisky ved hjælp af laserlysKredit:CC0 Public Domain Forskere fra University of St Andrews har udviklet en innovativ ny teknik ved hjælp af lasere til nøjagtigt at måle ægtheden af nogle af verdens mest eksklusive whiskyer
Verifikation af whisky ved hjælp af laserlysKredit:CC0 Public Domain Forskere fra University of St Andrews har udviklet en innovativ ny teknik ved hjælp af lasere til nøjagtigt at måle ægtheden af nogle af verdens mest eksklusive whiskyer -
 Forskere skubber mikroskopi til sub-molekylær opløsningAt være i stand til at se den indre funktion af de grundlæggende enheder i alt stof er virkelig fantastisk, og det er et af hovedmålene, vi har forfulgt hos CaSTL i mere end et årti, ” siger studie me
Forskere skubber mikroskopi til sub-molekylær opløsningAt være i stand til at se den indre funktion af de grundlæggende enheder i alt stof er virkelig fantastisk, og det er et af hovedmålene, vi har forfulgt hos CaSTL i mere end et årti, ” siger studie me -
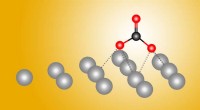 En sølvkugle til kemisk omdannelse af kuldioxidForskere opdager et overraskende første trin i den kemiske transformation af kuldioxid ved hjælp af en sølvkatalysator. Kredit:Berkeley Lab Fossile brændstoffer er livsnerven i moderne samfund, me
En sølvkugle til kemisk omdannelse af kuldioxidForskere opdager et overraskende første trin i den kemiske transformation af kuldioxid ved hjælp af en sølvkatalysator. Kredit:Berkeley Lab Fossile brændstoffer er livsnerven i moderne samfund, me
- Forskning kommer igennem med glans
- Hvilken rolle i indsnævring i et termometer?
- Forskere viser, hvordan man bruger topologiske pincet til at kontrollere aktive væsker
- Molekylære mekanismer for gydevaner for adaptiv stråling af endemiske østasiatiske cyprinidfisk
- Spørgsmål og svar:Hvad er det næste for OL i Tokyo, når virus spreder sig?
- Er brint et sjældent grundstof i universet som helhed?


