Aluminium og saltsyrereaktion:kemi forklaret
Reaktionen:
2 Al (s) + 6 HCl (aq) → 2 AlCl3 (aq) + 3 H2 (g)
Hvad sker der:
* Aluminium reagerer med saltsyre. Hydrogenionerne (H+) i syren angriber aluminiumsatomerne, fjerner elektroner og danner aluminiumioner (Al3+).
* Brandgas frigives. Elektronerne frigivet fra aluminiumsatomerne kombineres med brintioner og danner brintgas (H2), som bobler op.
* Der dannes aluminiumchlorid. Aluminiumionerne (Al3+) og chloridionerne (Cl-) fra syren kombineres og danner aluminiumchlorid (AlCl3), som opløses i opløsningen.
Observationer:
* Bubbling: Du vil se, at der dannes bobler på overfladen af aluminium. Dette er den brintgas, der frigives.
* Opløsning: Aluminiummetallet vil langsomt opløses, når det reagerer med syren.
* Varmeudvikling: Reaktionen er eksoterm, hvilket betyder, at den frigiver varme. Opløsningen kan blive varm.
Sikkerhed:
* Saltsyre er ætsende. Bær passende sikkerhedsudstyr, inklusive handsker, beskyttelsesbriller og en laboratoriefrakke.
* Brintgas er brandfarlig. Udfør ikke dette eksperiment i et lukket rum.
Anvendelser:
Denne reaktion bruges i forskellige applikationer, herunder:
* Rengøring: Rengøring af metaller, fjernelse af rust og ætsning af overflader.
* Produktion: Fremstilling af aluminiumchlorid, der anvendes i forskellige industrielle processer.
* Laboratorium: Påvisning af kemiske reaktioner og undersøgelse af metallers og syres egenskaber.
Bemærk: Reaktionshastigheden afhænger af faktorer som koncentrationen af syren, overfladearealet af aluminium og temperaturen.
 Varme artikler
Varme artikler
-
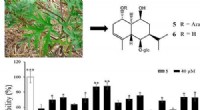 Ambrosie-forbindelser kunne beskytte nerveceller mod AlzheimersKredit:American Chemical Society Når foråret kommer på den nordlige halvkugle, mange mennesker forbander ragweed, en primær synder i sæsonbestemte allergier. Men videnskabsmænd har måske opdaget e
Ambrosie-forbindelser kunne beskytte nerveceller mod AlzheimersKredit:American Chemical Society Når foråret kommer på den nordlige halvkugle, mange mennesker forbander ragweed, en primær synder i sæsonbestemte allergier. Men videnskabsmænd har måske opdaget e -
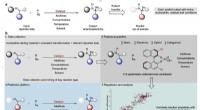 Forbedring af oddsene for syntetisk kemi succesProcessen til at udvikle prædiktive modeller for kemiske reaktioner. Kredit:Jolene Reid og Matthew Sigman. Kemi er mere end blot at blande forbindelse A med forbindelse B for at fremstille forbind
Forbedring af oddsene for syntetisk kemi succesProcessen til at udvikle prædiktive modeller for kemiske reaktioner. Kredit:Jolene Reid og Matthew Sigman. Kemi er mere end blot at blande forbindelse A med forbindelse B for at fremstille forbind -
 Præcis test af ethanolindhold:En praktisk vejledningAf bidragyder – Opdateret 24. marts 2022 Ethanol er et af de mest udbredte industrielle opløsningsmidler, der optræder i alt fra medicin og produkter til personlig pleje til drikkevarer og brændstoff
Præcis test af ethanolindhold:En praktisk vejledningAf bidragyder – Opdateret 24. marts 2022 Ethanol er et af de mest udbredte industrielle opløsningsmidler, der optræder i alt fra medicin og produkter til personlig pleje til drikkevarer og brændstoff -
 Brug af elektricitet til at nedbryde forurenende stoffer efter spildevandsrensningKredit:CC0 Public Domain Pesticider, farmaceutiske produkter, og hormonforstyrrende stoffer er nye forurenende stoffer, der ofte findes i renset husspildevand, selv efter sekundær behandling. Prof
Brug af elektricitet til at nedbryde forurenende stoffer efter spildevandsrensningKredit:CC0 Public Domain Pesticider, farmaceutiske produkter, og hormonforstyrrende stoffer er nye forurenende stoffer, der ofte findes i renset husspildevand, selv efter sekundær behandling. Prof
- Hvad er 300 ml i decimaler?
- Hvad skal videnskabsmanden gøre, hvis hans hypotese ikke er korrekt?
- Ingeniører gør et gyldent gennembrud for at forbedre elektroniske enheder
- Hvad sker der gravitationskraft for tiltrækning mellem to objekt, hvis masse en er halveret?
- Sådan beregnes reaktionshastighed
- Hvad er kernen og overfladesammensætningen af Mars?


