Adskillelse af opløselige faste stoffer fra væsker:metoder og teknikker
Forstå udfordringen
Når et fast stof opløses i en væske, danner det en homogen blanding kaldet en opløsning. De faste partikler bliver jævnt fordelt i væsken, hvilket gør dem umulige at adskille ved simple fysiske midler som filtrering.
Metoder til adskillelse
1. Fordampning
* Sådan virker det: Opvarm opløsningen. Væsken vil fordampe og efterlade det faste stof som en rest.
* Bedst til: Opløsninger, hvor det faste stof er stabilt ved væskens kogepunkt.
2. Destillation
* Sådan virker det: Opvarm opløsningen. Væsken vil fordampe, men opsamles derefter separat ved kondensering. Det faste stof forbliver i den originale beholder.
* Bedst til: Opløsninger, hvor det faste stof ikke er flygtigt (ikke let fordamper).
3. Krystallisering
* Sådan virker det: Afdamp forsigtigt opløsningsmidlet (væsken) fra opløsningen. Efterhånden som opløsningen bliver mere koncentreret, vil det faste stof begynde at krystallisere ud af opløsningen.
* Bedst til: Opløsninger, hvor det faste stof danner veldefinerede krystaller.
4. Kromatografi
* Sådan virker det: Denne teknik adskiller komponenter baseret på deres forskellige affiniteter for en stationær fase (som papir) og en mobil fase (som et opløsningsmiddel). Det er mere komplekst end de andre metoder.
* Bedst til: Komplekse blandinger, men ikke altid praktisk til simple faststof-væske-separationer.
Faktorer at overveje
* Faststoffets og væskens art: Overvej deres egenskaber (kogepunkt, opløselighed, flygtighed) for at vælge den mest passende metode.
* Ønsket resultat: Vil du genvinde det faste stof, væsken eller begge dele?
Eksempel
Lad os sige, at du har en opløsning af salt (NaCl) opløst i vand (H2O). Sådan kan du adskille dem:
* Fordampning: Opvarm opløsningen, indtil vandet fordamper, og efterlader saltet.
* Krystallisering: Fordamp langsomt vandet, så saltet kan krystallisere ud af opløsningen.
Bemærk: Nogle adskillelser kan være mere udfordrende end andre, og den specifikke metode, du vælger, vil afhænge af de specifikke involverede stoffer.
 Varme artikler
Varme artikler
-
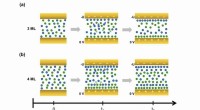 Forskere udvikler realtidsteknik til at studere ioniske væsker ved elektrodegrænsefladerTeamets forskning viste, at de ioniske rekonfigurationer, der forekommer nær guldelektroderne (gule stænger), afhænger af tykkelsen af de undersøgte ioniske flydende film, som illustreret i ovenståe
Forskere udvikler realtidsteknik til at studere ioniske væsker ved elektrodegrænsefladerTeamets forskning viste, at de ioniske rekonfigurationer, der forekommer nær guldelektroderne (gule stænger), afhænger af tykkelsen af de undersøgte ioniske flydende film, som illustreret i ovenståe -
 Automatiseret optimering og syntese af lægemidler i skyenKredit:Angewandte Chemie International Edition Shopping på internettet, lagring af billeder i skyen, skruer op for en termostat med en app – alt er almindeligt. Nu, tingenes internet og skyen komm
Automatiseret optimering og syntese af lægemidler i skyenKredit:Angewandte Chemie International Edition Shopping på internettet, lagring af billeder i skyen, skruer op for en termostat med en app – alt er almindeligt. Nu, tingenes internet og skyen komm -
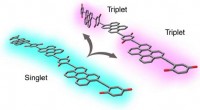 To-til-en energi fra fotoner, nu bedre end nogensindeVed at vride, når man er ophidset, nogle lange kæder af organiske molekyler kan isolere triplet excitoner i modsatte ender af molekylet. Kredit:National Renewable Energy Laboratory Ved vridning og
To-til-en energi fra fotoner, nu bedre end nogensindeVed at vride, når man er ophidset, nogle lange kæder af organiske molekyler kan isolere triplet excitoner i modsatte ender af molekylet. Kredit:National Renewable Energy Laboratory Ved vridning og -
 Flydende krystallers overraskende styrkeForskere er et skridt tættere på at udvikle længerevarende og sikrere batterier ved hjælp af flydende krystaller. Kredit:Pixabay Dendritter er de ødelæggende biprodukter af cyklussen med opladning
Flydende krystallers overraskende styrkeForskere er et skridt tættere på at udvikle længerevarende og sikrere batterier ved hjælp af flydende krystaller. Kredit:Pixabay Dendritter er de ødelæggende biprodukter af cyklussen med opladning
- Hvordan E. coli passerer sikkert gennem mavesyre
- Konverterer en generator bevægelsesenergi til elektrisk energi?
- Hvad kaldes en smal jordstrækning?
- Hvad er hårceller næret af?
- De grønneste spil nogensinde? Hvordan påstande om olympisk bæredygtighed rammer et rev på Tahiti…
- Hvilket af disse kemikalier er et vigtigt fotosyntetisk pigment i planter?


