Zinkoxidation:Forstå reaktionen og zinkoxiddannelsen
Reaktionen:
* Zink (Zn) + Oxygen (O2) → Zinkoxid (ZnO)
Hvad sker der:
1. Oxidation: Zink mister elektroner (oxideres) og bliver til en positivt ladet zinkion (Zn²⁺).
2. Reduktion: Ilt optager elektroner (blir reduceret) og bliver til negativt ladede oxidioner (O²⁻).
3. Danning af zinkoxid: De positivt ladede zinkioner og negativt ladede oxidioner tiltrækker hinanden og danner en stabil forbindelse kaldet zinkoxid (ZnO).
Karakteristika for reaktionen:
* Eksotermisk: Reaktionen frigiver varme, hvilket gør metallet varmt.
* Danning af en hvid belægning: Zinkoxid er et hvidt, pulveragtigt stof, der danner et beskyttende lag på overfladen af zinkmetallet. Dette lag forhindrer yderligere oxidation og beskytter zinken mod korrosion.
* Reaktionshastighed: Reaktionshastigheden afhænger af faktorer som temperatur, overfladeareal og tilstedeværelsen af fugt.
Anvendelser af zinkoxid:
Zinkoxid er en alsidig forbindelse med adskillige anvendelser, herunder:
* Solblokering: Anvendes som aktiv ingrediens i solcremer på grund af dens evne til at absorbere UV-stråler.
* Pigment: Anvendes som hvidt pigment i maling, gummi og plast.
* Medicinske anvendelser: Findes i salver og cremer til behandling af hudsygdomme som bleudslæt og acne.
* Industrielle anvendelser: Anvendes i forskellige industrielle processer, herunder fremstilling af gummi, klæbemidler og keramik.
Opsummering: Reaktionen mellem zink og ilt resulterer i dannelsen af zinkoxid, et hvidt beskyttende lag, der forhindrer yderligere korrosion. Denne reaktion er eksoterm og har mange praktiske anvendelser.
Sidste artikelVandmolekyle-elektronkonfiguration:Forstå ensomme par
Næste artikelZinkkarbonatnedbrydning:Producerer zinkoxid
 Varme artikler
Varme artikler
-
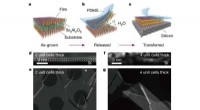 Forskere finder en måde at producere fritstående film af perovskitoxiderVækst og overførsel af ultratynde fritstående SrTiO3 -film. en, Skematisk af en film med et SAO -bufferlag. b, Det opofrende SAO -lag opløses i vand for at frigive de øverste oxidfilm med mekanisk und
Forskere finder en måde at producere fritstående film af perovskitoxiderVækst og overførsel af ultratynde fritstående SrTiO3 -film. en, Skematisk af en film med et SAO -bufferlag. b, Det opofrende SAO -lag opløses i vand for at frigive de øverste oxidfilm med mekanisk und -
 Reparation af aktivt pumpende hjertevæv med muslinge-inspireret vævsklæberInspireret af Moder Natur:Havmuslinger modstår let de stormfulde brændinger. De holder på overfladen med proteintråde. Empa-forskere bruger denne egenskab til en ny vævslim til sårbehandling. Kredit:P
Reparation af aktivt pumpende hjertevæv med muslinge-inspireret vævsklæberInspireret af Moder Natur:Havmuslinger modstår let de stormfulde brændinger. De holder på overfladen med proteintråde. Empa-forskere bruger denne egenskab til en ny vævslim til sårbehandling. Kredit:P -
 Hvad sker der i eksergoniske kemiske reaktioner? En ekspertguide til Gibbs Free EnergyAf John Brennan Opdateret 30. august 2022 Gibbs Free Energy Gibbs frie energi måler et systems kapacitet til at udføre ikke-mekanisk arbejde. Når Gibbs frie energi af reaktanter overstiger produkter
Hvad sker der i eksergoniske kemiske reaktioner? En ekspertguide til Gibbs Free EnergyAf John Brennan Opdateret 30. august 2022 Gibbs Free Energy Gibbs frie energi måler et systems kapacitet til at udføre ikke-mekanisk arbejde. Når Gibbs frie energi af reaktanter overstiger produkter -
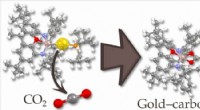 Det første nukleofile guldkompleksEn ny aluminium-guldforbindelse (til venstre) reagerer med kuldioxid ved indsættelse (til højre), hvilket viser guldatomets nukleofile karakter. Kredit:Jyväskylä Universitet En forskningsindsats m
Det første nukleofile guldkompleksEn ny aluminium-guldforbindelse (til venstre) reagerer med kuldioxid ved indsættelse (til højre), hvilket viser guldatomets nukleofile karakter. Kredit:Jyväskylä Universitet En forskningsindsats m
- Hvorfor har en kop, der sidder på bordet potentiel energi?
- Depolarisering ville forekomme ..... A-natriumkationer forlader cellen B-potassium C-chlorid-anioner…
- Ny indsigt i stjernedannelse i de mindste galakser
- Hvorfor sociale mediefirmaer vil kæmpe for at følge nye EU-regler om ulovligt indhold
- Reguleringen af fødevarer eller vandstand inde i en organismerceller for eksempel?
- Hvordan man forbedrer rumlige forhold for voksne


