Hvad sker der i eksergoniske kemiske reaktioner? En ekspertguide til Gibbs Free Energy
Af John Brennan
Opdateret 30. august 2022
Gibbs Free Energy
Gibbs frie energi måler et systems kapacitet til at udføre ikke-mekanisk arbejde. Når Gibbs frie energi af reaktanter overstiger produkternes, er reaktionen eksergonisk - termodynamisk spontan og i stand til at frigive energi uden ekstern input.
Eksoterm vs. eksergonisk
Mens mange eksergoniske reaktioner er eksoterme og udsender varme, er de to begreber forskellige. En eksergonisk proces kan endda absorbere varme (endotermisk), hvis den samlede entropiændring opvejer entalpiændringen. Tegnet på den frie energiændring, ikke varmestrømmen, bestemmer spontaniteten.
Entropi vs. Entalpi
Kemikere fra det 19. århundrede kæmpede med spontane endoterme reaktioner, fordi de overså entropi, målet for utilgængelig energi. En proces bliver eksergonisk, når den totale entropi af systemet plus omgivelser øges, selvom systemet selv absorberer varme.
Overvejelser
Reaktioner, der producerer en gas eller involverer fordampning, udviser typisk store positive entropiændringer, hvilket gør dem mere eksergoniske ved højere temperaturer. Omvendt er varmeafgivende reaktioner normalt mere eksergoniske ved lavere temperaturer. Reaktionskinetik har også betydning; en eksergonisk reaktion kan stadig være kinetisk træg og praktisk talt ikke observerbar.
 Varme artikler
Varme artikler
-
 Metode til at spore reaktioner mellem luft og kulstofbaserede forbindelser etableretGabriel Isaacman-VanWertz ankom til Virginia Tech for lidt over et år siden, men den nye adjunkt tog forskning med sig, der kan ændre den måde, forskere studerer luft på. Kredit:Virginia Tech Ved
Metode til at spore reaktioner mellem luft og kulstofbaserede forbindelser etableretGabriel Isaacman-VanWertz ankom til Virginia Tech for lidt over et år siden, men den nye adjunkt tog forskning med sig, der kan ændre den måde, forskere studerer luft på. Kredit:Virginia Tech Ved -
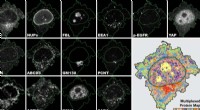 Ny metode forfiner celleprøveanalyse4i er den første billeddannelsesteknik, som giver os en multiplekset væv-til-organel-visning af biologiske prøver og forbinder flere oplysninger i et og samme eksperiment. Kredit:UZH Forskere ved
Ny metode forfiner celleprøveanalyse4i er den første billeddannelsesteknik, som giver os en multiplekset væv-til-organel-visning af biologiske prøver og forbinder flere oplysninger i et og samme eksperiment. Kredit:UZH Forskere ved -
 Ny katalysator forvandler forurenende stoffer til brændstofHaotian Wang, hvem vil slutte sig til Rice fakultetet senere i år, er hovedforfatter til en undersøgelse, der skal omdanne kuldioxid til kulilte og andre industrielle brændstoffer. Kredit:Jon Chase/Ha
Ny katalysator forvandler forurenende stoffer til brændstofHaotian Wang, hvem vil slutte sig til Rice fakultetet senere i år, er hovedforfatter til en undersøgelse, der skal omdanne kuldioxid til kulilte og andre industrielle brændstoffer. Kredit:Jon Chase/Ha -
 Hvad forårsager nedbrydning af genopladeligt batteri? Afhænger af, hvor mange gange du har opkræv…Kredit:CC0 Public Domain Genopladelige lithium-ion-batterier holder ikke evigt - efter nok cyklusser med opladning og genopladning vil de til sidst gå kaput, så forskere leder konstant efter måder
Hvad forårsager nedbrydning af genopladeligt batteri? Afhænger af, hvor mange gange du har opkræv…Kredit:CC0 Public Domain Genopladelige lithium-ion-batterier holder ikke evigt - efter nok cyklusser med opladning og genopladning vil de til sidst gå kaput, så forskere leder konstant efter måder
- Hvilket ord beskriver en organisme, der har genotypen BB?
- Forskellen mellem ortologe og parogene gener
- Marine hvirvelløse dyr har støjende menneskelige naboer
- Silicon Valleys sexismeproblem:Kan strømmen være ved at vende?
- Hvilken farve har himlen, når der ikke er skyer?
- Hvad er meningen med jordbunden?


