Mestring af Lewis Dot Structures:Sådan tælles valenselektroner for ethvert element
Af Sean Lancaster
Opdateret 30. august 2022
Lewis-punktdiagrammer giver en kortfattet visuel repræsentation af valens-elektronfordeling i kovalente molekyler, hvilket giver kemikere mulighed for hurtigt at vurdere bindingsmønstre. Nøjagtig konstruktion af en Lewis-struktur kræver viden om atomets valenselektroner. Det periodiske system arrangerer grundstoffer efter kemisk lighed; dets layout afspejler valens-elektrontal, hvor s-blokken (kolonne 1-2) og p-blokken (kolonne 13-18) viser de valensorbitaler, der indgår i kovalent binding.
Trin 1
Find grundstoffet i det periodiske system. Dens position afslører antallet af valenselektroner, som er grundlaget for ethvert Lewis-punktdiagram.
Trin 2
Skriv grundstoffets kemiske symbol. De fleste atomer kan rumme op til otte valenselektroner; brint og helium holder to. Overgangsmetaller kan acceptere op til atten elektroner, men alligevel afviger de ofte fra oktetreglen og danner komplekse koordinationsforbindelser.
Trin 3
Arranger valensorbitaler omkring symbolet. For enkeltbundne atomer placeres orbitalerne symmetrisk på hver side af symbolet. Dobbeltbindinger er repræsenteret af to elektroner i en af de tre orbitaler med 120°-afstand; tripelbindinger involverer tre elektroner i et lineært arrangement. Hver orbital kan rumme op til to elektroner.
Trin 4
Tæl elementets gruppenummer. I det periodiske system angiver de to første (s-blok) og sidste seks (p-blok) kolonner valenselektronantal. Overgangsmetaller (d-blok) indeholder også valenselektroner, selvom deres bindingsadfærd er mere kompleks.
Trin 5
Fordel valenselektronerne. Tildel en elektron pr. orbital, indtil alle orbitaler er optaget enkeltvis, og tilføj derefter den anden elektron til den samme orbital, hvis det kræves. For dobbelt- eller tredobbeltbindinger er de delte elektroner placeret mellem de to bundne atomer.
 Varme artikler
Varme artikler
-
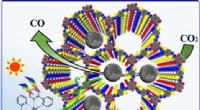 Ny undersøgelse belyser design af heterogene katalysatorer til selektiv kuldioxidfotoreduktionKredit:WANG Ruihus gruppe Anvendelse af kovalente organiske rammer (COFer) som heterogene katalysatorer for fotokatalytisk CO 2 reduktion har tiltrukket sig betydelig opmærksomhed på grund af de
Ny undersøgelse belyser design af heterogene katalysatorer til selektiv kuldioxidfotoreduktionKredit:WANG Ruihus gruppe Anvendelse af kovalente organiske rammer (COFer) som heterogene katalysatorer for fotokatalytisk CO 2 reduktion har tiltrukket sig betydelig opmærksomhed på grund af de -
 Forskere fremmer stamcelleterapi med biologisk nedbrydeligt stilladsEt biologisk nedbrydeligt uorganisk nano-stillads, bestående af stamceller, proteiner og lægemidler, til avanceret stamcelleterapi og lægemiddellevering. Kredit:KiBum Lee, Letao Yang og Sy-Tsong Dean
Forskere fremmer stamcelleterapi med biologisk nedbrydeligt stilladsEt biologisk nedbrydeligt uorganisk nano-stillads, bestående af stamceller, proteiner og lægemidler, til avanceret stamcelleterapi og lægemiddellevering. Kredit:KiBum Lee, Letao Yang og Sy-Tsong Dean -
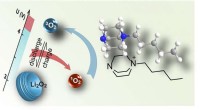 Batteriforskning:nye gennembrud inden for forskning i superbatterierDannelsen af singlet oxygen (1O2) forringer cyklusstabiliteten af mange alkalimetalkatoder, såsom Li-O2 katoden. I tidsskriftet præsenterer Angewandte Chemie Freunberger en effektiv og højspænding
Batteriforskning:nye gennembrud inden for forskning i superbatterierDannelsen af singlet oxygen (1O2) forringer cyklusstabiliteten af mange alkalimetalkatoder, såsom Li-O2 katoden. I tidsskriftet præsenterer Angewandte Chemie Freunberger en effektiv og højspænding -
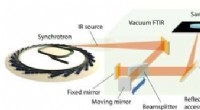 Undersøgelse af de komplekse dielektriske egenskaber af metal-organiske rammer (MOF'er)Figur 1:Den eksperimentelle opsætning til måling af bredbånds-IR-reflektiviteten af polykrystallinske MOF-pellets. De opnåede højopløsningsreflektivitetsdata blev efterfølgende brugt til at bestemme
Undersøgelse af de komplekse dielektriske egenskaber af metal-organiske rammer (MOF'er)Figur 1:Den eksperimentelle opsætning til måling af bredbånds-IR-reflektiviteten af polykrystallinske MOF-pellets. De opnåede højopløsningsreflektivitetsdata blev efterfølgende brugt til at bestemme
- Isotoper og neutroner:Forståelse af atomvariationer
- Krill giver indsigt i, hvordan marine arter kan tilpasse sig varmere farvande
- Hvad ville være den bedste isolator kulstof eller silicium aluminium oxygen?
- Hvilke af disse enheder bruger forskere til at måle ejendomsbevægelsen?
- Forbud mod genopbygning i katastrofeudsatte områder ignorerer boligejernes præferencer - at øge o…
- Hvilken akse vipper har planeterne i solsystemet?


