Anioner i ionisk binding:Hvordan ikke-metaller danner negative ioner
* Elektronegativitet: Ikke-metaller har højere elektronegativitet end metaller. Det betyder, at de har en stærkere tiltrækning af elektroner.
* Elektronforstærkning: Ved ionbinding vil et ikke-metalatom få en eller flere elektroner fra et metalatom for at opnå en stabil elektronkonfiguration (normalt en fuld ydre skal).
* Negativ debitering: Ved at få elektroner bliver ikke-metalatomet negativt ladet og danner en anion.
Eksempler på almindelige ikke-metalanioner:
* Halogener (Gruppe 17): Fluor (F-), Klorid (Cl-), Bromid (Br-), Jodid (I-)
* Oxygen (Gruppe 16): Oxid (O2-)
* Nitrogen (Gruppe 15): Nitrid (N3-)
* Svovl (Gruppe 16): Sulfid (S2-)
* Fosfor (Gruppe 15): Fosfid (P3-)
Vigtig bemærkning: Mens de fleste anioner er dannet af ikke-metaller, findes der nogle undtagelser. For eksempel kan visse polyatomiske ioner være negativt ladede og indeholde både metaller og ikke-metaller.
Sidste artikelAnioner i ionisk binding:Forståelse af ikke-metal adfærd
Næste artikelIonformel for aluminiumoxid (Al₂O₃) - kemi forklaret
 Varme artikler
Varme artikler
-
 Nyligt udviklet enzym fremskynder langsom organisk reaktionKredit:SUWIT NGAOKAEW, Shutterstock Alsidige katalysatorer med nye funktioner og funktioner kan revolutionere videnskabsmænds syntetiske strategier og bane vejen for kemikalier af høj værdi og en g
Nyligt udviklet enzym fremskynder langsom organisk reaktionKredit:SUWIT NGAOKAEW, Shutterstock Alsidige katalysatorer med nye funktioner og funktioner kan revolutionere videnskabsmænds syntetiske strategier og bane vejen for kemikalier af høj værdi og en g -
 At tænke uden for buret:En ny tilgang til energiintensive molekylære adskillelserKAUST-forskere udvikler organiske burlignende materialer til at adskille xylenisomerer på en mere energieffektiv måde. Kredit:KAUST; Anastasia Serin En omvendt form for vært-gæstekemi kunne hæmme
At tænke uden for buret:En ny tilgang til energiintensive molekylære adskillelserKAUST-forskere udvikler organiske burlignende materialer til at adskille xylenisomerer på en mere energieffektiv måde. Kredit:KAUST; Anastasia Serin En omvendt form for vært-gæstekemi kunne hæmme -
 Hård kærlighed:Intens genskin hjælper næste generations solteknologi gennem den akavede fase660 nm) er fra fase-separeret perovskit drevet af lav-intensitet konfokal mikroskop scanning laser. Kredit:ARC Center of Excellence in Exciton Science Forskere i Australien har løst en grundlæggen
Hård kærlighed:Intens genskin hjælper næste generations solteknologi gennem den akavede fase660 nm) er fra fase-separeret perovskit drevet af lav-intensitet konfokal mikroskop scanning laser. Kredit:ARC Center of Excellence in Exciton Science Forskere i Australien har løst en grundlæggen -
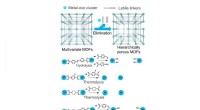 Strategier til at generere større porer i metal-organiske rammerIntroduktion af mesoporer i mikroporøse multivariate MOFer ved selektivt at fjerne labile linkere gennem hydrolyse, termolyse og ozonolyse. Gengivet fra Chem. Soc. Rev., 2019, 48, 4823-4853 med tillad
Strategier til at generere større porer i metal-organiske rammerIntroduktion af mesoporer i mikroporøse multivariate MOFer ved selektivt at fjerne labile linkere gennem hydrolyse, termolyse og ozonolyse. Gengivet fra Chem. Soc. Rev., 2019, 48, 4823-4853 med tillad
- Hvilke materialer eller genstande er 20 grader celsius?
- Hvilken kraft får sten til at ændre form?
- Forklar, om en bil kan bevæge sig med skiftende hastighed, mens den opretholder konstant hastighed?…
- Hvor meget større end Antares er solen?
- I reaktionen mellem brom og natrium får et atom en elektron og danner ion Br. hvad sker der med bro…
- Forsuring af havet vil øge jodindholdet i spiselige tang og deres forbrugere


