Forståelse af OH-koncentration i svovlsyreopløsninger
Sådan forstår du OH⁻-koncentrationen i en svovlsyreopløsning:
* Første ionisering: H2SO4 ioniserer fuldstændigt i vand og donerer en proton til dannelse af HSO4 - (hydrogensulfation) og H3O + (hydroniumion).
* H2SO4 (vandigt) + H2O (l) → HSO4- (vandigt) + H3O+ (vandigt)
* Anden ionisering: HSO4⁻ ioniserer også, men i mindre grad, donerer en anden proton for at danne SO₄²⁻ (sulfation) og en anden H₃O⁺.
* HSO₄⁻ (aq) + H₂O (l) ⇌ SO₄²⁻ (aq) + H3O⁺ (aq)
Den høje koncentration af H₃O⁺-ioner sænker OH⁻-koncentrationen betydeligt på grund af ionproduktkonstanten for vand (Kw):
*Kw =[H₃O⁺][OH⁻] =1,0 × 10⁻14 ved 25°C
Derfor er OH⁻-koncentrationen i en svovlsyreopløsning ekstremt lav. For at beregne den nøjagtige værdi skal du kende koncentrationen af svovlsyreopløsningen og overveje begge ioniseringstrin.
Nøglepunkter:
* Svovlsyre er en stærk syre, hvilket betyder, at den ioniserer fuldstændigt i opløsning.
* Tilstedeværelsen af H₃O⁺-ioner fra syren reducerer OH⁻-koncentrationen betydeligt.
* Den nøjagtige OH⁻-koncentration afhænger af koncentrationen af svovlsyreopløsningen.
 Varme artikler
Varme artikler
-
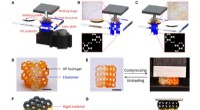 3D-udskrivning meget strækbar hydrogel med forskellige UV-hærdbare polymererMultimateriale 3D -printhydrogel med andre polymerer. (A) Illustration af det DLP-baserede multimateriale 3D-udskrivningsapparat. (B og C) Processer til udskrivning af elastomer- og hydrogelstrukturer
3D-udskrivning meget strækbar hydrogel med forskellige UV-hærdbare polymererMultimateriale 3D -printhydrogel med andre polymerer. (A) Illustration af det DLP-baserede multimateriale 3D-udskrivningsapparat. (B og C) Processer til udskrivning af elastomer- og hydrogelstrukturer -
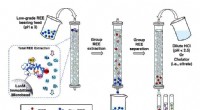 Ny, miljøvenlig metode til at udvinde og adskille sjældne jordarterLavkvalitetskilder til sjældne jordarters grundstoffer (REE), fra industriaffald, indeholder typisk mange sjældne jordarters grundstoffer og andre metaller blandet sammen. En ny ekstraktions- og separ
Ny, miljøvenlig metode til at udvinde og adskille sjældne jordarterLavkvalitetskilder til sjældne jordarters grundstoffer (REE), fra industriaffald, indeholder typisk mange sjældne jordarters grundstoffer og andre metaller blandet sammen. En ny ekstraktions- og separ -
 Koder smart antibiotikaKredit:National Physical Laboratory En metode til at designe antibiotika baseret på tilfældig binær kodning, udviklet af et team ledet af National Physical Laboratory (NPL), kunne åbne op for nye
Koder smart antibiotikaKredit:National Physical Laboratory En metode til at designe antibiotika baseret på tilfældig binær kodning, udviklet af et team ledet af National Physical Laboratory (NPL), kunne åbne op for nye -
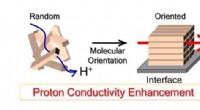 Få mere kontrol over brændselscellemembranerMolekylær orientering forbedrer protonkonduktion i protonkonduktive polymerer. Kredit:Yuki Nagao Mere organisering på molekylært niveau kan forbedre effektiviteten af membraner, der bruges i bri
Få mere kontrol over brændselscellemembranerMolekylær orientering forbedrer protonkonduktion i protonkonduktive polymerer. Kredit:Yuki Nagao Mere organisering på molekylært niveau kan forbedre effektiviteten af membraner, der bruges i bri
- Sådan bruges et nummer Line
- Gødning forårsager mere end 2 % af de globale emissioner
- Hvad gør kernen i en stjerne, når den blæser sin overflade ud i rummet for at danne planetarisk t…
- Indtager stoffer nogen plante- eller dyrecelle ved at passere gennem en membran?
- Hvordan man gør det muligt for insiders sociale forandringsagenter at tackle og miljøproblemer i o…
- Hvilken er dannet af befrugtning af æg i embryosæk?


