Molekylær bevægelse:Forståelse af kinetisk energi og materiens tilstande
Her er hvorfor:
* Temperatur og kinetisk energi: Jo højere temperatur et stof har, jo hurtigere bevæger dets molekyler sig. Dette skyldes, at temperatur er et mål for den gennemsnitlige kinetiske energi af molekylerne.
* Bevægelsestyper: Bevægelsestypen afhænger af stoffets tilstand:
* Gasser: Molekyler bevæger sig frit og tilfældigt i alle retninger og kolliderer med hinanden og væggene i deres beholder.
* Væsker: Molekyler er stadig i bevægelse, men de er tættere pakket end i gasser. De kan glide forbi hinanden, så væsker kan flyde.
* Fast: Molekyler i faste stoffer vibrerer omkring faste positioner, men de har stadig kinetisk energi. De holdes sammen af stærke intermolekylære kræfter, der forhindrer dem i at bevæge sig frit.
* Nulpunktsenergi: Selv ved det absolutte nulpunkt (0 Kelvin) har molekyler stadig en lille mængde vibrationsenergi, kendt som nulpunktsenergi.
Opsummering: Molekylær bevægelse er en grundlæggende egenskab ved stof, og den er afgørende for at forstå stoffers adfærd i forskellige tilstande.
 Varme artikler
Varme artikler
-
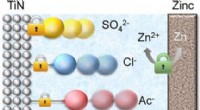 Zink-ion-hybridkondensatorer med ideelle anioner i elektrolytten viser ekstra lang ydelseKredit:Wiley Metal-ion hybrid kondensatorer kombinerer egenskaberne af kondensatorer og batterier. En elektrode bruger den kapacitive mekanisme, den anden redox-processer af batteritype. Forskere
Zink-ion-hybridkondensatorer med ideelle anioner i elektrolytten viser ekstra lang ydelseKredit:Wiley Metal-ion hybrid kondensatorer kombinerer egenskaberne af kondensatorer og batterier. En elektrode bruger den kapacitive mekanisme, den anden redox-processer af batteritype. Forskere -
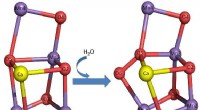 Mekanisme for fotosyntetisk vandopdeling afsløret af en røntgenfri elektronlaserFigur 1:Strukturelle ændringer af Mn4CaO5-klyngen induceret af to lysglimt. S1-tilstand:uden belysning; S3-tilstand:efter to lysglimt. Kredit:Okayama University Fotosystem II (PSII) er et enormt m
Mekanisme for fotosyntetisk vandopdeling afsløret af en røntgenfri elektronlaserFigur 1:Strukturelle ændringer af Mn4CaO5-klyngen induceret af to lysglimt. S1-tilstand:uden belysning; S3-tilstand:efter to lysglimt. Kredit:Okayama University Fotosystem II (PSII) er et enormt m -
 En praktisk guide til deionisering af vand til laboratorier og hverdagsbrugAf Allan Robinson | Opdateret 24. marts 2022 Deioniseret vand er et hjørnestensopløsningsmiddel i kemi og mange daglige anvendelser. Ved at fjerne ladede ioner – kationer og anioner – kan forskere fo
En praktisk guide til deionisering af vand til laboratorier og hverdagsbrugAf Allan Robinson | Opdateret 24. marts 2022 Deioniseret vand er et hjørnestensopløsningsmiddel i kemi og mange daglige anvendelser. Ved at fjerne ladede ioner – kationer og anioner – kan forskere fo -
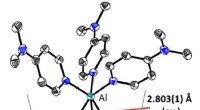 Vigtig milepæl på vejen mod overgangsmetalkatalyse med aluminiumKredit:Albert-Ludwigs-Universität Freiburg im Breisgau Kemikerne Philipp Dabringhaus, Julie Willrett og Prof. Dr. Ingo Krossing fra Institut for Uorganisk og Analytisk Kemi ved Universitetet i Frei
Vigtig milepæl på vejen mod overgangsmetalkatalyse med aluminiumKredit:Albert-Ludwigs-Universität Freiburg im Breisgau Kemikerne Philipp Dabringhaus, Julie Willrett og Prof. Dr. Ingo Krossing fra Institut for Uorganisk og Analytisk Kemi ved Universitetet i Frei
- Hvad er der blevet brugt i de sidste 150 år til at producere det meste af Worlds Energy?
- Hvordan skriver du 0,000002 i videnskabelig notation?
- Elementer i den europæiske industrirevolution
- At skifte fra centimeter til meter Hvordan flytter du decimalen?
- Forskning bidrager til politiske ændringer for at støtte arbejdere midt i COVID-19-pandemien
- Hvilke organeller er flere i aktive celler?


