Molalitet forklaret:Koncentration i kemi (m vs. M)
Her er en oversigt:
* Løsning: Stoffet opløses.
* Opløsningsmiddel: Stoffet, der opløser.
* Fuldvarpe: En måleenhed for mængden af stof, lig med 6,022 x 10^23 partikler (atomer, molekyler, ioner osv.).
Hvorfor bruge molalitet?
Molalitet foretrækkes frem for molaritet (mol opløst stof pr. liter *opløsning*) i visse situationer:
* Temperaturuafhængighed: Molalitet påvirkes ikke af temperaturændringer, i modsætning til molaritet, som ændres, når opløsningens volumen udvider eller trækker sig sammen.
* Koligative egenskaber: Molalitet bruges til at beregne kolligative egenskaber, som er egenskaber ved opløsninger, der afhænger af koncentrationen af opløste partikler. Eksempler omfatter frysepunktsdepression og kogepunktsforhøjelse.
Beregning af molalitet:
For at beregne molaliteten af en opløsning skal du vide:
* Moler opløst stof: Dette kan findes ved at dividere massen af opløst stof med dets molære masse.
* Opløsningsmiddelmasse i kilogram: Dette er normalt angivet direkte i opgaven, men du kan også beregne det ved at trække massen af opløst stof fra opløsningens samlede masse.
Eksempel:
Lad os sige, at du har en opløsning, der indeholder 0,5 mol NaCl opløst i 1 kg vand. Molaliteten af denne opløsning ville være:
Molalitet (m) =0,5 mol NaCl / 1 kg vand =0,5 mol/kg
Sammenfattet giver molalitet et pålideligt mål for koncentrationen, der er uafhængig af temperaturudsving og er afgørende for forståelsen af kolligative egenskaber ved opløsninger.
Sidste artikelElektropositive radikaler:symboler, værdier og egenskaber
Næste artikelForstå løsningskoncentration:Hvornår er de lige?
 Varme artikler
Varme artikler
-
 Ramanome-databasen kan hjælpe med at udvinde mikroalgecellefabrikker for at reducere kulstofemissio…Maskinindlæring af ramanomer hjælper med at screene mikroalgalcellefabrikker, der reparerer kuldioxid. Kredit:LIU Yang Mikroalger er simple organismer af enkeltceller, Alligevel giver de et stort
Ramanome-databasen kan hjælpe med at udvinde mikroalgecellefabrikker for at reducere kulstofemissio…Maskinindlæring af ramanomer hjælper med at screene mikroalgalcellefabrikker, der reparerer kuldioxid. Kredit:LIU Yang Mikroalger er simple organismer af enkeltceller, Alligevel giver de et stort -
 Forskere syntetiserer gipserstatningNaturlig gipssten. Kredit:Maksim Safaniuk Et internationalt hold af videnskabsmænd har foreslået en metode til fremstilling af højkvalitets gipsbindemidler baseret på syntetisk calciumsulfatdihydr
Forskere syntetiserer gipserstatningNaturlig gipssten. Kredit:Maksim Safaniuk Et internationalt hold af videnskabsmænd har foreslået en metode til fremstilling af højkvalitets gipsbindemidler baseret på syntetisk calciumsulfatdihydr -
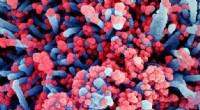 Forstå overfladekemien af SARS-CoV-2Farvelagt scanningselektronmikrofotografi af en celle (blå) stærkt inficeret med SARS-CoV-2-viruspartikler (rød), isoleret fra en patientprøve. Billede taget på NIAID Integrated Research Facility (IRF
Forstå overfladekemien af SARS-CoV-2Farvelagt scanningselektronmikrofotografi af en celle (blå) stærkt inficeret med SARS-CoV-2-viruspartikler (rød), isoleret fra en patientprøve. Billede taget på NIAID Integrated Research Facility (IRF -
 3D-printet materiale til erstatning af elfenben til restaurering af artefakterTil højre:Det nye materiale Digory; elfenben til venstre. Kredit:Vienna University of Technology I århundreder, elfenben blev ofte brugt til at lave kunstgenstande. Men for at beskytte elefantpopu
3D-printet materiale til erstatning af elfenben til restaurering af artefakterTil højre:Det nye materiale Digory; elfenben til venstre. Kredit:Vienna University of Technology I århundreder, elfenben blev ofte brugt til at lave kunstgenstande. Men for at beskytte elefantpopu
- Sådan fungerer spontan menneskelig forbrænding
- Teenage sexting:Svigtede unge mennesker ved ikke at tale om det
- NASA finder vindskæring påvirket nye Tropical Cyclone 09S
- Hvis man kender massen og molæret af reaktant, kan et produkt D i en kemisk reaktion bestemme produ…
- Hvad er den kemiske formel for mannose?
- Hvad er Jupiters Volcanic Moon?


