Hvis man kender massen og molæret af reaktant, kan et produkt D i en kemisk reaktion bestemme produceret ved hjælp af?
1. Afbalanceret kemisk ligning:
* Du har brug for den afbalancerede kemiske ligning for reaktionen. Dette fortæller dig molforholdet mellem reaktant A og produkt D.
2. Molmasse:
* Du har brug for de molære masser af både reaktant A og produkt D. Dette er massen af en mol af hvert stof (normalt findes på den periodiske tabel).
3. Konverteringstrin:
* Trin 1:Konverter masse af reaktant A til mol: Del den givne masse af en ved dens molære masse.
* Trin 2:Brug molforholdet: Multiplicer molen af A med molforholdet fra den afbalancerede ligning (mol D / mol A). Dette giver dig molen af produkt D dannet.
* Trin 3:Konverter mol af D til masse: Multiplicer molen af D med dens molære masse.
Eksempel:
Lad os sige, at du har følgende reaktion:
2 a -> d
Og du ved:
* Masse på A =10 gram
* Molmasse på A =50 g/mol
* Molmasse d =100 g/mol
Beregninger:
1. mol af A: 10 g / 50 g / mol =0,2 mol
2. mol D: 0,2 mol A * (1 mol d / 2 mol a) =0,1 mol d
3. Masse D: 0,1 mol d * 100 g/mol =10 gram
Derfor produceres 10 gram produkt D fra 10 gram reaktant A.
Sidste artikelHvad har flere ydre elektroner fosfor eller silicium?
Næste artikelHvad er den kemiske formel for bly IV -ion?
 Varme artikler
Varme artikler
-
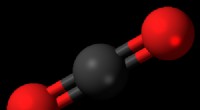 Forsker undersøger, hvordan man konverterer kuldioxid til byggestenene til brændstofBall-and-stick model af kuldioxid. Kredit:Wikipedia At opdele de kemiske bindinger i CO2 molekyler, er der brug for varme. En måde at få denne varme på er fra plasmaer, og det har længe været kendt
Forsker undersøger, hvordan man konverterer kuldioxid til byggestenene til brændstofBall-and-stick model af kuldioxid. Kredit:Wikipedia At opdele de kemiske bindinger i CO2 molekyler, er der brug for varme. En måde at få denne varme på er fra plasmaer, og det har længe været kendt -
 Hvorfor er visse tungmetaller okay at spise? (video)Kredit:The American Chemical Society Tungmetaller har ry for at være farlige, men nogle er essentielle næringsstoffer, som du ikke kan leve uden. I denne uges afsnit af Reaktioner , undersøger vi h
Hvorfor er visse tungmetaller okay at spise? (video)Kredit:The American Chemical Society Tungmetaller har ry for at være farlige, men nogle er essentielle næringsstoffer, som du ikke kan leve uden. I denne uges afsnit af Reaktioner , undersøger vi h -
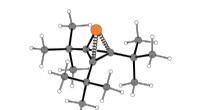 Fjederbelastet system sætter fosfor ind i molekylære ringeBilledtekst:MIT-kemikere opdagede en måde at inkorporere fosfor i tre-leddede ringforbindelser ved at bruge dette fjederbelastede molekyle som kilden til fosfor. Kreditering:Udlånt af forskerne MIT
Fjederbelastet system sætter fosfor ind i molekylære ringeBilledtekst:MIT-kemikere opdagede en måde at inkorporere fosfor i tre-leddede ringforbindelser ved at bruge dette fjederbelastede molekyle som kilden til fosfor. Kreditering:Udlånt af forskerne MIT -
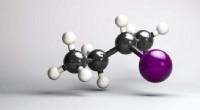 Iagttager ændringer i molekylernes chiralitet i realtidKirale molekyler - forbindelser, der er spejlbilleder af hinanden - spiller en vigtig rolle i biologiske processer og i kemisk syntese. Kemikere ved ETH Zürich er nu lykkedes for første gang at bruge
Iagttager ændringer i molekylernes chiralitet i realtidKirale molekyler - forbindelser, der er spejlbilleder af hinanden - spiller en vigtig rolle i biologiske processer og i kemisk syntese. Kemikere ved ETH Zürich er nu lykkedes for første gang at bruge
- Delvis solformørkelse synlig over hele Storbritannien
- Hvad er den elektricitet, der produceres ved at producere?
- El Nino og afslutningen på den globale opvarmning
- Utilstrækkelig beskyttelse af kvinder og piger, der søger tilflugt i Tyskland
- Opsving begynder efter stormen hærger indiske, Bangladesh kyst
- Billede:Noctis Labyrinthus stereopar


