Forståelse af hydrofobicitet:Identifikation af de mest vandafvisende molekyler
* Perfluorcarboner (PFC'er): Disse er forbindelser, der kun indeholder kulstof- og fluoratomer. Fluors høje elektronegativitet skaber en meget stærk ikke-polær binding med kulstof, hvilket gør PFC'er ekstremt hydrofobe. Eksempler inkluderer perfluoroctan (C8F18) og perfluordecalin (C10F18).
* Mættede kulbrinter: Disse molekyler består kun af kulstof- og brintatomer forbundet med enkeltbindinger. De mangler polære grupper og er derfor meget hydrofobe. Eksempler inkluderer methan (CH4), ethan (C2H6) og hexan (C6H14).
* Alifatiske kæder: Lange kæder af kulstof- og brintatomer, almindelige i fedtstoffer og olier, er generelt hydrofobe.
Det er vigtigt at bemærke, at:
* Hydrofobicitet er et spektrum: Der er ikke en klar linje, der opdeler molekyler i "hydrofobe" og "hydrofile". I stedet udviser molekyler en række hydrofobiciteter.
* Hydrofobicitet er kontekstafhængig: Et molekyles hydrofobicitet kan påvirkes af faktorer såsom opløsningsmidlet, det er i, temperaturen og tilstedeværelsen af andre molekyler.
Så mens PFC'er og mættede kulbrinter er blandt de mest hydrofobe molekyler, er det ikke muligt at erklære et enkelt "mest hydrofobt" molekyle uden at specificere konteksten.
 Varme artikler
Varme artikler
-
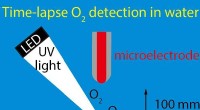 Hurtigere detektion af fotokatalysator-genereret oxygen har store konsekvenser for ren energiFigur 1:Påvisning af oxygen (O2) genereret fra kunstig fotosyntese ved hjælp af en mikroelektrode. Kredit:Kobe University I øjeblikket, størstedelen af den energi, der forbruges af verdens befol
Hurtigere detektion af fotokatalysator-genereret oxygen har store konsekvenser for ren energiFigur 1:Påvisning af oxygen (O2) genereret fra kunstig fotosyntese ved hjælp af en mikroelektrode. Kredit:Kobe University I øjeblikket, størstedelen af den energi, der forbruges af verdens befol -
 Et enkelt fingeraftryk på gerningsstedet opdager stofmisbrug i klasse AKredit:CC0 Public Domain National Center of Excellence in Mass Spectrometry Imaging hos NPL, i samarbejde med University of Surrey og Ionoptika Ltd afslører de seneste fund, der viser, hvordan et
Et enkelt fingeraftryk på gerningsstedet opdager stofmisbrug i klasse AKredit:CC0 Public Domain National Center of Excellence in Mass Spectrometry Imaging hos NPL, i samarbejde med University of Surrey og Ionoptika Ltd afslører de seneste fund, der viser, hvordan et -
 Den perfekte blanding:Optimering af gasblandinger til brintlagring i clathrathydraterForskere finder optimal hydrogen-naturgasblanding til at fange brint i burlignende molekyler mere effektivt. Kredit:GIST I vores igangværende søgen efter at forvandle sig til et mere miljøvenligt
Den perfekte blanding:Optimering af gasblandinger til brintlagring i clathrathydraterForskere finder optimal hydrogen-naturgasblanding til at fange brint i burlignende molekyler mere effektivt. Kredit:GIST I vores igangværende søgen efter at forvandle sig til et mere miljøvenligt -
 Kemikere finder nye måder at nedbryde gamle dæk til materiale til nyeKandidatstuderende Sijia Zheng afbilledet med Michael Brook fra McMaster University Kredit:Georgia Kirkos, McMaster University Et team af kemikere ved McMaster University har opdaget en innovativ
Kemikere finder nye måder at nedbryde gamle dæk til materiale til nyeKandidatstuderende Sijia Zheng afbilledet med Michael Brook fra McMaster University Kredit:Georgia Kirkos, McMaster University Et team af kemikere ved McMaster University har opdaget en innovativ
- Hvad er nogle ligheder og forskelle mellem fysisk kemisk forvitring?
- Uddybende spørgsmål:Er sociale netværkssider nyttige for erhvervslivet?
- Genealogier af Mayflower-passagerer hjælper med at finde efterkommere
- Hvad betyder Wall Streets genopretning for Main Street?
- Fem forskellige typer vejrkort
- Hvad er betegnelsen for et estimat af den mængde energi, der er nødvendig for at opretholde grundl…


