Forståelse af vandmolekylebinding:kovalente bindinger og polaritet
* Deling af elektroner: Hvert brintatom har en elektron i sin yderste skal, mens oxygen har seks. For at opnå en stabil konfiguration deler de elektroner. Oxygenatomet deler en elektron med hvert brintatom og danner to kovalente bindinger.
* Polaritet: Ilt er mere elektronegativt end brint, hvilket betyder, at det trækker de delte elektroner tættere på sig selv. Dette skaber en delvis negativ ladning på oxygenatomet og delvis positiv ladning på hydrogenatomerne. Dette gør vandmolekylet polært , med en positiv ende og en negativ ende.
Tiltrækningen mellem de delvist positive brintatomer i et vandmolekyle og det delvist negative oxygenatom i et andet vandmolekyle kaldes en hydrogenbinding.
Brintbindinger er svagere end kovalente bindinger, men de er stadig vigtige, fordi de:
* Hold vandmolekyler sammen: Dette giver vand dets høje overfladespænding og gør det muligt at eksistere som en væske ved stuetemperatur.
* Tillad vand at opløse mange stoffer: Vandmolekylernes polaritet hjælper dem med at bryde ioniske forbindelser fra hinanden og tiltrække polære molekyler.
* Spille en afgørende rolle i biologiske processer: Hydrogenbindinger er essentielle for at opretholde strukturen af proteiner, DNA og andre biologiske molekyler.
 Varme artikler
Varme artikler
-
 Skaller og grapefrugter inspirerer til først fremstillet ikke-skærbart materialeKredit:CC0 Public Domain Ingeniører har hentet deres inspiration fra skaller og grapefrugter til at skabe, hvad de siger er det første fremstillede ikke-skærbare materiale. Dette nye materiale, s
Skaller og grapefrugter inspirerer til først fremstillet ikke-skærbart materialeKredit:CC0 Public Domain Ingeniører har hentet deres inspiration fra skaller og grapefrugter til at skabe, hvad de siger er det første fremstillede ikke-skærbare materiale. Dette nye materiale, s -
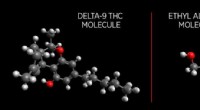 Forskere lægger grunden til en pålidelig marihuana -alkometerEn af grundene til, at det er svært at designe en pålidelig marihuana-alkometer er, at delta-9 tetrahydrocannabinol (THC), den primære psykoaktive forbindelse i marihuana, er et stort molekyle med man
Forskere lægger grunden til en pålidelig marihuana -alkometerEn af grundene til, at det er svært at designe en pålidelig marihuana-alkometer er, at delta-9 tetrahydrocannabinol (THC), den primære psykoaktive forbindelse i marihuana, er et stort molekyle med man -
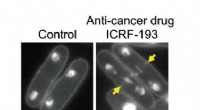 Anticancer-mekanisme afsløret i gæreksperimenterMed DNA topoisomerase II (topo II) intakt, DNA i fissionsgærceller replikeres normalt og deles jævnt mellem to datterceller (venstre). Når det er under virkningen af anti-cancer lægemidlet ICRF-193,
Anticancer-mekanisme afsløret i gæreksperimenterMed DNA topoisomerase II (topo II) intakt, DNA i fissionsgærceller replikeres normalt og deles jævnt mellem to datterceller (venstre). Når det er under virkningen af anti-cancer lægemidlet ICRF-193, -
 Byg en 3-D Carbon Atom Model:En trin-for-trin uddannelsesvejledningAf Kristy King – Opdateret 30. august 2022 Ingram Publishing/Ingram Publishing/Getty Images At forstå atomstruktur er grundlæggende for kemi, og kulstof – livets rygrad – er et tilgængeligt eksempel
Byg en 3-D Carbon Atom Model:En trin-for-trin uddannelsesvejledningAf Kristy King – Opdateret 30. august 2022 Ingram Publishing/Ingram Publishing/Getty Images At forstå atomstruktur er grundlæggende for kemi, og kulstof – livets rygrad – er et tilgængeligt eksempel
- At stoppe koalaudryddelsen er pinefuldt simpelt, men her er grunden til, at jeg ikke er optimistisk
- Hvordan kan du fortælle, at en høj dykker har gravitationspotentiale energi?
- Hvad er nylige forskningsresultater understøtter Darwins -teori om evolution?
- Hvordan kunne du se, om et topografisk kort viser gradvis hældning?
- Seksuel reproduktion:En omfattende oversigt over kønsceller og befrugtning
- Termonukleare flammer:Astrofysikere bruger supercomputer til at udforske eksotiske stjernefænomener…


