Ioniske sammensætningsformler:Forståelse af forholdet mellem ioner
* Ioniske forbindelser: Ioniske forbindelser dannes af den elektrostatiske tiltrækning mellem positivt ladede ioner (kationer) og negativt ladede ioner (anioner).
* Balancerende gebyrer: For at danne en stabil forbindelse skal den samlede positive ladning svare til den samlede negative ladning. Dette opnås ved at finde det mindste hele antal forhold mellem kationer og anioner, der balancerer ladningerne.
* Eksempel: Overvej natriumchlorid (NaCl). Natrium (Na) danner en +1 ion (Na+) og klor (Cl) danner en -1 ion (Cl-). For at balancere ladningerne skal vi bruge en Na+ ion for hver en Cl-ion, hvilket resulterer i formlen NaCl.
Her er en mere detaljeret forklaring:
1. Identificer ionerne: Bestem ladningerne af kationer og anioner involveret i forbindelsen. Du kan bruge det periodiske system eller en liste over almindelige ioner til at hjælpe dig.
2. Find det mindste fælles multiplum (LCM): Ladningernes LCM vil bestemme antallet af hver ion, der er nødvendig.
3. Juster abonnenterne: Divider LCM med ladningen af hver ion for at bestemme subscriptet for den ion i formlen.
Eksempel:Magnesiumoxid (MgO)
* Magnesium (Mg) danner en +2 ion (Mg2+)
* Ilt (O) danner en -2 ion (O2-)
* LCM for +2 og -2 er 2.
* Vi har brug for en Mg2+ ion (2/2 =1) og en O2-ion (2/2 =1) for at balancere ladningerne.
* Derfor er formlen for magnesiumoxid MgO.
Nøglepunkter:
* Forholdet i en ionforbindelse er altid det enkleste hele talforhold, der balancerer ladningerne.
* Du kan bruge en metode på kryds og tværs til hurtigt at bestemme subskripterne i en ionisk forbindelse.
* Forholdet er ofte repræsenteret som en kemisk formel, som NaCl eller MgO.
Sig til, hvis du vil øve dig med flere eksempler!
 Varme artikler
Varme artikler
-
 SkumbruserMicellære skumfilm viser gråtoneintensitetsvariationer, der svarer til rig nanoskopisk topografi kortlagt ved hjælp af IDIOM-protokoller. Kredit:Chrystian Ochoa og Vivek Sharma Kemiske ingeniører
SkumbruserMicellære skumfilm viser gråtoneintensitetsvariationer, der svarer til rig nanoskopisk topografi kortlagt ved hjælp af IDIOM-protokoller. Kredit:Chrystian Ochoa og Vivek Sharma Kemiske ingeniører -
 MRI-scanning hjælper med næste generations batteridesignKredit:CC0 Public Domain Magnetisk resonansbilleddannelse (MRI) kan give en effektiv måde at understøtte udviklingen af den næste generation af højtydende genopladelige batterier, ifølge forskni
MRI-scanning hjælper med næste generations batteridesignKredit:CC0 Public Domain Magnetisk resonansbilleddannelse (MRI) kan give en effektiv måde at understøtte udviklingen af den næste generation af højtydende genopladelige batterier, ifølge forskni -
 Bioengineer har til formål at forvandle naturens virusbekæmpere til kraftfulde stofferKredit:CC0 Public Domain Blandt de kraftfulde biokemikalier i det menneskelige immunsystem, peptider er en af de bedste. Findes oftest på de steder, hvor mikrober elsker at slå rod - øjets slim
Bioengineer har til formål at forvandle naturens virusbekæmpere til kraftfulde stofferKredit:CC0 Public Domain Blandt de kraftfulde biokemikalier i det menneskelige immunsystem, peptider er en af de bedste. Findes oftest på de steder, hvor mikrober elsker at slå rod - øjets slim -
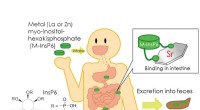 Kemisk kompleks kan øge udskillelsen af radioaktivt strontium fra kroppenDer er en hypotese om, at M-InsP6 kunne forbedre elimineringen af radiostrontium. M-InsP6 kan binde radiostrontium, hæmmer absorption, og øge udskillelsen. Kredit:Kanazawa University 90 Sr (t1
Kemisk kompleks kan øge udskillelsen af radioaktivt strontium fra kroppenDer er en hypotese om, at M-InsP6 kunne forbedre elimineringen af radiostrontium. M-InsP6 kan binde radiostrontium, hæmmer absorption, og øge udskillelsen. Kredit:Kanazawa University 90 Sr (t1
- Hvad er princippet om inkluderingstilstand i geologi for at relatere til klipper?
- Bekymret for elevernes mentale sundhed? Hvordan wellness er relateret til akademisk præstation
- Hvilken er den laveste del af den menneskelige hjerne?
- Små, medikamentfyldte bobler fører til tredobbelt angrebsbehandling for leverkræft
- Beskriv Hvordan forekommer nedbør, og hvad bestemmer, at typen af det falder på jorden?
- Hvad er det samme mellem forvitring og erosion?


