Forståelse af 92-graders bindingsvinklen i hydrogensulfid (H₂S)
1. Lone Pair Repulsion:
* Svovl i H₂S har to ensomme elektronpar foruden de to bindingspar med brintatomer.
* Ensomme par optager mere plads end bindingspar på grund af deres højere elektrontæthed.
* Disse enlige par udøver stærkere frastødende kræfter på bindingsparrene, skubber brintatomerne tættere sammen og mindsker H-S-H-bindingsvinklen.
2. Hybridisering:
* Svovlatomet i H₂S er sp³-hybridiseret, hvilket betyder, at det har fire orbitaler med samme energiniveau.
* De to ensomme par optager dog to af disse orbitaler, hvilket kun efterlader to til binding med brint.
* Denne hybridisering fører til en forvrænget tetraedrisk geometri med en mindre bindingsvinkel.
3. Mindre størrelse af hydrogenatom:
* Brintatomer er meget små sammenlignet med svovl.
* Denne lille størrelse gør det muligt for brintatomerne at være tættere på hinanden, hvilket yderligere bidrager til den mindre bindingsvinkel.
4. Fravær af stærke intermolekylære kræfter:
* H₂S er et polært molekyle, men det har relativt svage intermolekylære kræfter på grund af den lave elektronegativitetsforskel mellem brint og svovl.
* Denne mangel på stærke intermolekylære kræfter gør det muligt for molekylet at antage en mere afslappet konformation med en mindre bindingsvinkel.
Sammenfattende bidrager kombinationen af lone-par repulsion, sp³-hybridisering, den lille størrelse af hydrogen og svage intermolekylære kræfter til 92-graders bindingsvinklen i hydrogensulfid.
 Varme artikler
Varme artikler
-
 Ny undersøgelse bekræfter bølget arkproteinstruktur forudsagt i 1953Det krusede betaark er en variation af det plisserede betaark, et velkendt strukturelt motiv, der findes i tusindvis af proteiner. Linus Pauling og Robert Corey beskrev det krusede beta-ark i 1953, me
Ny undersøgelse bekræfter bølget arkproteinstruktur forudsagt i 1953Det krusede betaark er en variation af det plisserede betaark, et velkendt strukturelt motiv, der findes i tusindvis af proteiner. Linus Pauling og Robert Corey beskrev det krusede beta-ark i 1953, me -
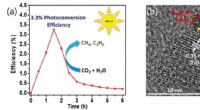 En-to-punch katalysatorer, der fanger kuldioxid til renere brændstofferBrændstofproduktionseffektivitet af titaniumdioxid fotokatalysator med kobber-platin legering co-katalysator (a) og et foto af fotokatalysator observeret af HRTEM (b) Kredit:©DGIST Kobber- og plat
En-to-punch katalysatorer, der fanger kuldioxid til renere brændstofferBrændstofproduktionseffektivitet af titaniumdioxid fotokatalysator med kobber-platin legering co-katalysator (a) og et foto af fotokatalysator observeret af HRTEM (b) Kredit:©DGIST Kobber- og plat -
 Nye muligheder for lysemitterende plast med mønstret lysMønstret lys i form af en fisk. Kredit:Mattias Lindh Lysemitterende plast bruges i dag i tv- og smartphone-skærme, lysemitterende indikatorer og som belysning til biler og fly med særlige krav. Vi
Nye muligheder for lysemitterende plast med mønstret lysMønstret lys i form af en fisk. Kredit:Mattias Lindh Lysemitterende plast bruges i dag i tv- og smartphone-skærme, lysemitterende indikatorer og som belysning til biler og fly med særlige krav. Vi -
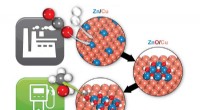 Chemists ID katalytisk nøgle til omdannelse af CO2 til methanolBrookhaven-forskere har identificeret, hvordan en zink/kobber (Zn/Cu) katalysator omdanner kuldioxid (to røde og en grå kugler) og brint (to hvide kugler) til methanol (en grå, en rød, og fire hvide k
Chemists ID katalytisk nøgle til omdannelse af CO2 til methanolBrookhaven-forskere har identificeret, hvordan en zink/kobber (Zn/Cu) katalysator omdanner kuldioxid (to røde og en grå kugler) og brint (to hvide kugler) til methanol (en grå, en rød, og fire hvide k


