Kul vs. diamant:Forstå forskellen på trods af fælles kulstofsammensætning
Her er en opdeling:
Kul:
* Struktur: Kul er en kompleks blanding af kulstof, brint, oxygen, nitrogen og svovl. Kulstofatomerne i kul er arrangeret i en tilfældig, uordnet struktur , der ofte danner kæder og plader.
* Binding: Bindingerne mellem kulstofatomer i kul er relativt svage.
* Egenskaber: På grund af sin uordnede struktur og svage bindinger er kul blødt, skørt og porøst . Det brænder let, hvilket gør det til en værdifuld brændstofkilde.
Diamant:
* Struktur: Diamantens kulstofatomer er arrangeret i et højt ordnet, tredimensionelt gitter kaldet en tetraedrisk struktur . Dette betyder, at hvert carbonatom er bundet til fire andre carbonatomer i et specifikt geometrisk mønster.
* Binding: Bindingerne mellem carbonatomer i diamant er meget stærke og kovalente .
* Egenskaber: Diamantens stive, stærke og tætpakkede struktur giver den exceptionelle egenskaber:
* Hårdhed: Diamant er det hårdeste naturligt forekommende materiale kendt.
* Højt brydningsindeks: Diamanter funkler strålende på grund af deres evne til at bryde lys.
* Høj varmeledningsevne: Diamanter leder varme meget godt.
* Kemisk inertitet: Diamanter er meget modstandsdygtige over for kemiske angreb.
Opsummering:
Mens både kul og diamant er lavet af kulstof, giver deres vidt forskellige strukturer og bindingsmønstre dem dramatisk forskellige egenskaber. Det er som at bygge et hus med de samme mursten, men at arrangere dem anderledes. Du kan ende med et hyggeligt sommerhus eller en storslået skyskraber!
Sidste artikelForståelse af 92-graders bindingsvinklen i hydrogensulfid (H₂S)
Næste artikelBrint og ilts vitale rolle i cellulær funktion
 Varme artikler
Varme artikler
-
 Omdannelse af kuldioxid til kulilte ved hjælp af vand, elektricitetReduktion af CO 2 . Kredit:Mr. Aditya Prajapati Forskere ved University of Illinois i Chicago og Joint Center for Artificial Photosynthesis har fastslået, hvordan elektrokatalysatorer kan omdann
Omdannelse af kuldioxid til kulilte ved hjælp af vand, elektricitetReduktion af CO 2 . Kredit:Mr. Aditya Prajapati Forskere ved University of Illinois i Chicago og Joint Center for Artificial Photosynthesis har fastslået, hvordan elektrokatalysatorer kan omdann -
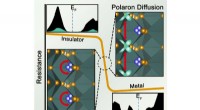 Team kaster nyt lys over design af uorganiske materialer til hjernelignende databehandlingFigur, der viser kobberionbevægelsen inden for et stift gitter af vanadium og ilt som kæden af en elektrisk ledningsevneændring i det kamæleonlignende materiale, der kan udnyttes til at skabe elektr
Team kaster nyt lys over design af uorganiske materialer til hjernelignende databehandlingFigur, der viser kobberionbevægelsen inden for et stift gitter af vanadium og ilt som kæden af en elektrisk ledningsevneændring i det kamæleonlignende materiale, der kan udnyttes til at skabe elektr -
 Forskere opnår 4-D trykt materialeForskerne printede deres silikone-baserede prøver ved hjælp af en direkte blæk-skriveproces. Det sammensatte blækmateriale blev ekstruderet ved stuetemperatur fra printerens dyse for at danne træbunke
Forskere opnår 4-D trykt materialeForskerne printede deres silikone-baserede prøver ved hjælp af en direkte blæk-skriveproces. Det sammensatte blækmateriale blev ekstruderet ved stuetemperatur fra printerens dyse for at danne træbunke -
 Forskere finder potentiel anvendelse for genbrugsplast i betonFra venstre, ingeniørfakultetet Adrienne Phillips, Cecily Ryan og Chelsea Heveran, sammen med doktorgradsstuderende Seth Kane og senior Michael Espinal viser prøver i deres laboratorium relateret til
Forskere finder potentiel anvendelse for genbrugsplast i betonFra venstre, ingeniørfakultetet Adrienne Phillips, Cecily Ryan og Chelsea Heveran, sammen med doktorgradsstuderende Seth Kane og senior Michael Espinal viser prøver i deres laboratorium relateret til
- Hvorfor bøjes lys, når det går gennem glas i en vinkel?
- Taler vi om Brexit - hvordan kom vi til dette punkt?
- Hvilken type væske bruger du i et termometer?
- Energikilde til det meste på jorden?
- 3 videnskabsmand, der smuglede i undersøgelse af biologi?
- Hvilken energitransformation forekommer med et jern?


