Ædelgasser:Elementer med fuld valensskaller - definition og egenskaber
Her er hvorfor:
* Valence Shell: Dette refererer til den yderste elektronskal af et atom.
* Ædelgasser: Disse er grundstoffer i gruppe 18 i det periodiske system (også kendt som gruppe VIIIA). De er kendt for at være meget ureaktive, fordi de har en fuld valensskal, hvilket betyder, at de ikke let får eller taber elektroner.
Undtagelser:
* Helium (Han) har kun 2 elektroner i sin valensskal, men den betragtes stadig som en ædelgas på grund af dens stabilitet.
* Brint (H) har 1 elektron i sin valensskal og betragtes ikke som en ædelgas.
Så selvom ikke alle grundstoffer med 2 eller 8 valenselektroner er ædelgasser, er udtrykket "ædelgas" ofte forbundet med denne egenskab på grund af deres unikke kemiske egenskaber.
 Varme artikler
Varme artikler
-
 Varmelagring:Forskere udvikler materiale, der er stabilt, effektivt og miljøvenligtFelix Marske har en prøve af det nye materiale. Kredit:Uni Halle / Marian Sorge Et nyt varmelagermateriale kan være med til at forbedre bygningers energieffektivitet markant. Udviklet af forskere v
Varmelagring:Forskere udvikler materiale, der er stabilt, effektivt og miljøvenligtFelix Marske har en prøve af det nye materiale. Kredit:Uni Halle / Marian Sorge Et nyt varmelagermateriale kan være med til at forbedre bygningers energieffektivitet markant. Udviklet af forskere v -
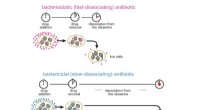 At lære antibiotika at være mere effektive dræbereForskning viser, at langvarig hæmning af proteinsyntese fører til celledød. Kredit:Proceedings of the National Academy of Sciences Forskning fra University of Illinois i Chicago tyder på bindingsv
At lære antibiotika at være mere effektive dræbereForskning viser, at langvarig hæmning af proteinsyntese fører til celledød. Kredit:Proceedings of the National Academy of Sciences Forskning fra University of Illinois i Chicago tyder på bindingsv -
 En videnskabelig metode til perfekt fondueKredit:American Chemical Society Ostefondue er et ikon for det schweiziske køkken og et hovedprodukt til middagsselskab. Selvom det kan virke som en simpel ret, at få den rigtige tekstur kan være
En videnskabelig metode til perfekt fondueKredit:American Chemical Society Ostefondue er et ikon for det schweiziske køkken og et hovedprodukt til middagsselskab. Selvom det kan virke som en simpel ret, at få den rigtige tekstur kan være -
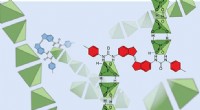 Skinner lys over den underlige verden af dihydrogenphosphatanionerRepræsentation, der viser dihydrogenphosphater (i grønt), der binder sammen i opløsning. Kredit:UNSW Forskere ved UNSW Sydney, sammen med samarbejdspartnere fra Western Sydney University og Hollan
Skinner lys over den underlige verden af dihydrogenphosphatanionerRepræsentation, der viser dihydrogenphosphater (i grønt), der binder sammen i opløsning. Kredit:UNSW Forskere ved UNSW Sydney, sammen med samarbejdspartnere fra Western Sydney University og Hollan
- Hvilket år kredsede John Glenn månen?
- Er det sandt, at tyngdekraften kun virker på genstande overfladen?
- Klimaændringer forårsager et dramatisk fald i den Persiske Golfs biodiversitet og fiskeripotential…
- Sådan fungerer månen
- Hvilket år var den første model af DNA?
- Hvorfor skulle regeringen udvikle alternative energikilder?


