Forståelse af hydrogen i reduktionsreaktioner:gevinst eller tab?
Her er en oversigt over hvorfor:
* Reduktion er defineret som forstærkningen af elektroner.
* Brint kan være involveret i reduktion på to måder:
* Tab af brint: I nogle reaktioner betyder fjernelse af hydrogenatomer (eller protoner, H+) fra et molekyle reduktion. Dette er typisk i organisk kemi, hvor reduktion ofte involverer tilsætning af hydrogen til en dobbelt- eller tredobbeltbinding.
* Forstærkning af brint: I andre tilfælde kan reduktion involvere *tilsætning* af hydrogenatomer til et molekyle. Dette sker ofte, når en metalion får elektroner, og hydrogenioner (H+) reduceres til at danne brintgas (H₂).
Eksempler:
* Tab af brint: Reduktionen af et aldehyd til en alkohol involverer tilsætning af to hydrogenatomer (H+) til carbonylgruppen. Dette er et klassisk eksempel på reduktion, hvor brint opnås.
* Gevinst af brint: Reduktionen af en metalion, som Fe³⁺ til Fe²⁺, kan forekomme i nærvær af hydrogengas. Brinten oxideres til H+, mens metalionen får elektroner.
Nøglepunkter:
* Reduktion handler om forstærkningen af elektroner, ikke nødvendigvis om tabet eller forstærkningen af brint.
* Den specifikke kemiske reaktion bestemmer, om brint er tabt eller opnået under reduktion.
Sig til, hvis du har andre spørgsmål!
Sidste artikelDichlormethan-densitet:hvorfor det synker i vand - forklaret
Næste artikelNettoladning af CH2:Forståelse af radikal stabilitet
 Varme artikler
Varme artikler
-
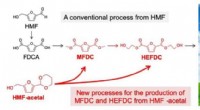 Grøn plastproduktion gjort letFigur 1. Reaktionsvej for produktion af MFDC og HEFDC fra HMF (en konventionel proces) og HMF-acetal (nye one-pot processer). Kredit:Kiyotaka Nakajima, Hokkaido Universitet En et-trins metode muli
Grøn plastproduktion gjort letFigur 1. Reaktionsvej for produktion af MFDC og HEFDC fra HMF (en konventionel proces) og HMF-acetal (nye one-pot processer). Kredit:Kiyotaka Nakajima, Hokkaido Universitet En et-trins metode muli -
 Visualisering af varmeflow i bambus kan hjælpe med at designe mere energieffektive og brandsikre by…Kredit:Pixabay Modificerede naturlige materialer vil være en væsentlig komponent i en bæredygtig fremtid, men først er der behov for en detaljeret forståelse af deres egenskaber. Måden varme strøm
Visualisering af varmeflow i bambus kan hjælpe med at designe mere energieffektive og brandsikre by…Kredit:Pixabay Modificerede naturlige materialer vil være en væsentlig komponent i en bæredygtig fremtid, men først er der behov for en detaljeret forståelse af deres egenskaber. Måden varme strøm -
 Forskere registrerer greenlight gasdetektering ved stuetemperaturSkyder. Kredit:MIPT Russiske forskere har udviklet en mekanisme til at detektere molekylært brint ved hjælp af grønt lys til at belyse en nanokrystallinsk sammensat sensor baseret på zink og indiu
Forskere registrerer greenlight gasdetektering ved stuetemperaturSkyder. Kredit:MIPT Russiske forskere har udviklet en mekanisme til at detektere molekylært brint ved hjælp af grønt lys til at belyse en nanokrystallinsk sammensat sensor baseret på zink og indiu -
 Højstyrke pultruderede termoplastiske kompositter lavet af nyt råmaterialeDet venstre foto viser fremstillingen af termoplastisk fladt laminat på en pultruderingsmaskine:Strimler af kildemateriale tilføres fra venstre, med kompositprofilerne trukket ud til højre. Det ande
Højstyrke pultruderede termoplastiske kompositter lavet af nyt råmaterialeDet venstre foto viser fremstillingen af termoplastisk fladt laminat på en pultruderingsmaskine:Strimler af kildemateriale tilføres fra venstre, med kompositprofilerne trukket ud til højre. Det ande
- Når en masse materiale bevæger sig ned ad buet langs overfladen kaldes processen?
- Hvad vil der ske med kuglerhastigheden, når den falder længere under relationspunktet?
- Arkæologer skal undgå forhistoriske Brexit-paralleller - de tilskynder til forskruede læsninger a…
- Hvad er forskellen mellem en prokaryotisk og eukary-otisk celle?
- Tågeharpe øger opsamlingskapaciteten for rent vand
- Er kraften øget til dobbelt så meget, når afstanden mellem to stjerner falder med halvdelen?


