Ionbindinger:Hvilke atomer danner dem og eksempler
1. Et metalatom: Metaller har en tendens til at miste elektroner og blive positivt ladede ioner (kationer).
2. Et ikke-metalatom: Ikke-metaller har tendens til at få elektroner og blive negativt ladede ioner (anioner).
Her er nogle eksempler:
* Natrium (Na) og klor (Cl): Natrium (et metal) mister en elektron for at blive Na+, og klor (et ikke-metal) får den elektron til at blive Cl-. Disse modsat ladede ioner tiltrækker hinanden og danner den ioniske forbindelse natriumchlorid (NaCl), almindeligvis kendt som bordsalt.
* Magnesium (Mg) og ilt (O): Magnesium (et metal) mister to elektroner for at blive Mg2+, og Oxygen (et ikke-metal) får to elektroner til at blive O2-. Dette resulterer i dannelsen af magnesiumoxid (MgO).
Husk: Nøglen er, at det ene atom skal have en stærk tendens til at miste elektroner, mens det andet har brug for en stærk tendens til at få elektroner.
 Varme artikler
Varme artikler
-
 Forskere bruger maskinlæringsteknik til hurtigt at evaluere nye overgangsmetalforbindelserResultater fra en analyse af kunstigt neuralt netværk (ANN) er muligvis ikke pålidelige for molekyler, der er for forskellige fra dem, som ANN blev trænet på. De sorte skyer, der er vist her, dækker o
Forskere bruger maskinlæringsteknik til hurtigt at evaluere nye overgangsmetalforbindelserResultater fra en analyse af kunstigt neuralt netværk (ANN) er muligvis ikke pålidelige for molekyler, der er for forskellige fra dem, som ANN blev trænet på. De sorte skyer, der er vist her, dækker o -
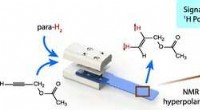 Nye lægemiddeltestforskninger kan drastisk reducere behovet for forsøgsdyrKredit:ACS Undersøgelser fra University of Southampton om en ny måde at teste lægemidler på kan væsentligt reducere behovet for forsøgsdyr. Professor Marcel Utz, Leder af magnetisk resonans ved u
Nye lægemiddeltestforskninger kan drastisk reducere behovet for forsøgsdyrKredit:ACS Undersøgelser fra University of Southampton om en ny måde at teste lægemidler på kan væsentligt reducere behovet for forsøgsdyr. Professor Marcel Utz, Leder af magnetisk resonans ved u -
 Forskerteam udvikler en ny klasse bløde materialerShifeng Nian og ph.d. studerende Jinchang Zhu ilægger blækket i en sprøjte til 3D -print. Kredit:University of Virginia Jeg tror, du er stille. Dette var den mest brugte sætning i 2020, ifølge H
Forskerteam udvikler en ny klasse bløde materialerShifeng Nian og ph.d. studerende Jinchang Zhu ilægger blækket i en sprøjte til 3D -print. Kredit:University of Virginia Jeg tror, du er stille. Dette var den mest brugte sætning i 2020, ifølge H -
 Forbedring af klæbemidler til bærbare sensorerEn film fremstillet af 4C3-PVA forblev klæbet til to grisehudsoverflader, når de blev adskilt (øverst); en umodificeret PVA-film gjorde det ikke (nederst). Kredit:Tilpasset fra ACS Omega 2020, DOI:1
Forbedring af klæbemidler til bærbare sensorerEn film fremstillet af 4C3-PVA forblev klæbet til to grisehudsoverflader, når de blev adskilt (øverst); en umodificeret PVA-film gjorde det ikke (nederst). Kredit:Tilpasset fra ACS Omega 2020, DOI:1
- Hvad er størrelsessammenligningen af Uranus og Merkur?
- Forskere skitserer en vision for en rentabel klimaændringsløsning
- Sådan beregnes enthalpy af Air
- Heks af følgende hjælper planter med at beskytte mod at blive spist?
- Er det at være i stand til fysisk at inspicere klipperne i mantel til en værdi af høje omkostning…
- Hvad er virkningen af varme på partikler?


