Forståelse af håndsæbe:pH, alkalinitet og rengøringsevne
Her er hvorfor:
* Sæbe fremstilles ved forsæbning: Denne proces involverer at reagere et fedtstof eller en olie med en stærk alkali (som lud eller kaliumhydroxid). De resulterende sæbemolekyler har et polært (vandelskende) hoved og en ikke-polær (olieelskende) hale.
* Alkalinitet hjælper med rengøring: Sæbens alkalinitet gør det muligt for den at nedbryde fedt og snavs, som ofte er sure.
* pH i sæbe: Mens den nøjagtige pH varierer, er håndsæbe generelt mellem 9 og 10, hvilket betragtes som basisk.
Det er dog vigtigt at bemærke:
* Der er nogle håndsæber, der er tættere på neutrale (pH 7), især dem, der markedsføres som "skånsomme" eller "til følsom hud."
* Sæbens pH kan også påvirkes af andre ingredienser tilføjet under fremstillingsprocessen.
Mens håndsæbe generelt er basisk, er der derfor en vis variation afhængigt af det specifikke produkt.
Sidste artikelKobber- og sølvnitratreaktion:forskydning og ordligning
Næste artikelIonbindinger:Hvilke atomer danner dem og eksempler
 Varme artikler
Varme artikler
-
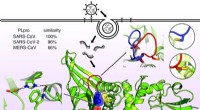 Information om molekylær form af vira, der forårsager COVID-19, SARS, og MERS afslører strukturel…Molekylær struktur af det papainlignende enzym kendt som PLPro. Dette enzym tillader de vira, der forårsager SARS, MERS, og COVID-19 for at inficere celler og replikere og undertrykke værtens immunfun
Information om molekylær form af vira, der forårsager COVID-19, SARS, og MERS afslører strukturel…Molekylær struktur af det papainlignende enzym kendt som PLPro. Dette enzym tillader de vira, der forårsager SARS, MERS, og COVID-19 for at inficere celler og replikere og undertrykke værtens immunfun -
 Nyt RNA-modificerende værktøj korrigerer genetiske sygdomme, herunder driver af triple-negativ bry…Professor Matthew Disney fra The Scripps Research Institute ledede den nye undersøgelse. Kredit:Scripps Research Institute Efterhånden som forskere får indsigt i, hvilke gener der driver sygdomme,
Nyt RNA-modificerende værktøj korrigerer genetiske sygdomme, herunder driver af triple-negativ bry…Professor Matthew Disney fra The Scripps Research Institute ledede den nye undersøgelse. Kredit:Scripps Research Institute Efterhånden som forskere får indsigt i, hvilke gener der driver sygdomme, -
 Kemikere syntetiserer flade siliciumforbindelser3D -repræsentation af et af de nye molekyler. Silikationer i tetraedrisk arrangement kan ses i de sfæriske sæbebobler til sammenligning. Kredit:Jens Rump / University of Bonn Kemikere ved universi
Kemikere syntetiserer flade siliciumforbindelser3D -repræsentation af et af de nye molekyler. Silikationer i tetraedrisk arrangement kan ses i de sfæriske sæbebobler til sammenligning. Kredit:Jens Rump / University of Bonn Kemikere ved universi -
 Sådan fortyndes kobbersulfat sikkert og præcistAf Pearl Lewis Opdateret 24. marts 2022 Kobbersulfat er et lyseblåt krystallinsk salt, der almindeligvis bruges i kemilaboratorier og pædagogiske eksperimenter. At fortynde det nøjagtigt er afgørende
Sådan fortyndes kobbersulfat sikkert og præcistAf Pearl Lewis Opdateret 24. marts 2022 Kobbersulfat er et lyseblåt krystallinsk salt, der almindeligvis bruges i kemilaboratorier og pædagogiske eksperimenter. At fortynde det nøjagtigt er afgørende


