Sådan fortyndes kobbersulfat sikkert og præcist
Af Pearl Lewis Opdateret 24. marts 2022
Kobbersulfat er et lyseblåt krystallinsk salt, der almindeligvis bruges i kemilaboratorier og pædagogiske eksperimenter. At fortynde det nøjagtigt er afgørende for at opnå den ønskede molaritet og for sikkerheden. Følgende vejledning skitserer en pålidelig, trin-for-trin metode til at omdanne en koncentreret kobbersulfatopløsning til en præcist defineret fortyndet opløsning.
Før du begynder, skal du sikre dig, at du har passende PPE – handsker, beskyttelsesbriller og en laboratoriefrakke – og arbejde i et godt ventileret område.
Trin 1 – Beregn fortyndingsfaktoren
Divider startkoncentrationen med målkoncentrationen. For eksempel, hvis du begynder med en 1.0moldm -3 løsning og ønsker at nå 0,1 moldm -3 , er fortyndingsfaktoren 1,0/0,1=10, ofte udtrykt som et forhold på 1:10.
Trin 2 – Bestem enhedsvolumen
Divider det endelige volumen, du har brug for, med fortyndingsfaktoren. For at forberede 500mL af den fortyndede opløsning er enhedsvolumenet 500mL/10=50mL.
Trin 3 – Overfør det opløste stof
Brug en kalibreret pipette til at trække nøjagtig en enhedsvolumen af stamopløsningen og tilsætte den til en ren målekolbe. I eksemplet ovenfor overføres 50 ml af 1,0 moldm -3 lager.
Trin 4 – Tilsæt destilleret vand
Beregn mængden af vand, der skal tilføjes:(fortyndingsfaktor–1)×enhed volumen. Tilsæt (10–1)×50mL=450mL vand for en faktor 10.
Trin 5 – Bland grundigt
Forsegl kolben med en prop og vend forsigtigt eller ryst, indtil opløsningen er homogen. Den resulterende blanding er nu den ønskede fortyndede kobbersulfatopløsning.
Påkrævede materialer
- Volumetrisk kolbe (f.eks. 500 ml)
- Stop
- Kalibreret pipette
- Destilleret eller deioniseret vand
Sidste artikelVidenskaben bag sukkerkrystaldannelse
Næste artikelBeregning af opløselighedsprocent:En trin-for-trin guide
 Varme artikler
Varme artikler
-
 Dekonstruktion af superfooden, der bestemmer honningbiernes hierarkiKredit:CC0 Public Domain Alle bilarver spiser royal gelé, når de er nye, men kun fremtidige dronninger fortsætter med at spise det. For at finde ud af hvorfor, forskere i Østrig ser nærmere på de
Dekonstruktion af superfooden, der bestemmer honningbiernes hierarkiKredit:CC0 Public Domain Alle bilarver spiser royal gelé, når de er nye, men kun fremtidige dronninger fortsætter med at spise det. For at finde ud af hvorfor, forskere i Østrig ser nærmere på de -
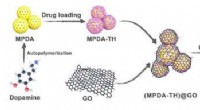 Cellulose nanofibril-baseret indkapslingsstruktur til at kontrollere lægemiddelfrigivelseDesignet af MPDA@GO/CNF-indkapslingsstrukturen og applikationen til kontrolleret lægemiddelfrigivelse. Kredit:LIU Yingying Intelligente hydrogeler med flere funktioner såsom vedvarende lægemiddelf
Cellulose nanofibril-baseret indkapslingsstruktur til at kontrollere lægemiddelfrigivelseDesignet af MPDA@GO/CNF-indkapslingsstrukturen og applikationen til kontrolleret lægemiddelfrigivelse. Kredit:LIU Yingying Intelligente hydrogeler med flere funktioner såsom vedvarende lægemiddelf -
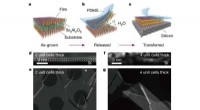 Forskere finder en måde at producere fritstående film af perovskitoxiderVækst og overførsel af ultratynde fritstående SrTiO3 -film. en, Skematisk af en film med et SAO -bufferlag. b, Det opofrende SAO -lag opløses i vand for at frigive de øverste oxidfilm med mekanisk und
Forskere finder en måde at producere fritstående film af perovskitoxiderVækst og overførsel af ultratynde fritstående SrTiO3 -film. en, Skematisk af en film med et SAO -bufferlag. b, Det opofrende SAO -lag opløses i vand for at frigive de øverste oxidfilm med mekanisk und -
 Anatomi af en acnebehandlingKredit:CC0 Public Domain Sarecyclin, et lægemiddel godkendt til brug i USA i 2018, er det første nye antibiotikum godkendt til behandling af acne i mere end 40 år. Nu, forskere ved Yale og Univers
Anatomi af en acnebehandlingKredit:CC0 Public Domain Sarecyclin, et lægemiddel godkendt til brug i USA i 2018, er det første nye antibiotikum godkendt til behandling af acne i mere end 40 år. Nu, forskere ved Yale og Univers
- Tilsløre adgangsmønstre for at beskytte følsomme data i skyen
- Hvad er den 1. Densest -satellit?
- Vil Google bringe held til Credit Karma?
- Midlertidige byløsninger hjælper os med at håndtere kriser – og kan føre til radikale skift i by…
- De længste levende stjerner er dem af?
- ORNL-teamet bygger bærbar diagnostik til fusionseksperimenter fra varer på hylden


