Ioniseringsenergi:Identifikation af atomet med den laveste elektronfjernelsesenergi
* Ioniseringsenergi: Den energi, der kræves for at fjerne den mest løst bundne elektron fra et gasformigt atom, kaldes ioniseringsenergi.
* Periodiske tendenser: Ioniseringsenergi stiger generelt, når du bevæger dig:
* På tværs af en periode (venstre mod højre): Atomer har et stærkere greb om deres elektroner på grund af stigende nuklear ladning.
* Op en gruppe (top til bund): Elektroner er længere væk fra kernen, hvilket gør dem nemmere at fjerne.
Lad os analysere mulighederne:
* Sn (Tin): Gruppe 14, periode 5
* Sr (Strontium): Gruppe 2, periode 5
* Vær (Beryllium): Gruppe 2, periode 2
* Br (Brom): Gruppe 17, periode 4
Begrundelse:
* Strontium (Sr) og Beryllium (Be): Begge er i gruppe 2 (jordalkalimetaller). Sr er længere nede i gruppen end Be, så dens yderste elektron er længere fra kernen og lettere at fjerne.
* Tin (Sn) og brom (Br): Sn er i gruppe 14, Br er i gruppe 17. Brom vil have en højere ioniseringsenergi på grund af dets større nukleare ladning og stærkere tiltrækning til dets elektroner.
Konklusion:
Baseret på periodiske tendenser, Strontium (Sr) kræver mindst energi for at fjerne dens mest løst bundne elektron.
Derfor er svaret (b).
Sidste artikelKoboltreaktivitet:egenskaber, faktorer og anvendelser
Næste artikelMercury:Elementet, der ikke let fordamper
 Varme artikler
Varme artikler
-
 Produktionsteknologi for nye flystrukturer har øget deres styrke3D-printede kompositdele. Kredit:Sergey Gnuskov/NUST MISIS Forskere fra NUST MISIS har udviklet en metode til fremstilling af kompositdele til luftfartsindustrien, som har øget styrken af færdige
Produktionsteknologi for nye flystrukturer har øget deres styrke3D-printede kompositdele. Kredit:Sergey Gnuskov/NUST MISIS Forskere fra NUST MISIS har udviklet en metode til fremstilling af kompositdele til luftfartsindustrien, som har øget styrken af færdige -
 Nyt elektrodedesign kan føre til kraftigere batterierKredit:CC0 Public Domain Ny forskning fra ingeniører ved MIT og andre steder kan føre til batterier, der kan pakke mere strøm pr. pund og holde længere, baseret på det længe søgte mål om at bruge
Nyt elektrodedesign kan føre til kraftigere batterierKredit:CC0 Public Domain Ny forskning fra ingeniører ved MIT og andre steder kan føre til batterier, der kan pakke mere strøm pr. pund og holde længere, baseret på det længe søgte mål om at bruge -
 At tælle alkanisomerer:en praktisk vejledningAf Kevin Beck | Opdateret 24. marts 2022 Hvad er isomerer? Isomerer er forbindelser, der deler den samme molekylære formel, men adskiller sig i struktur eller rumlig arrangement. De falder i to hov
At tælle alkanisomerer:en praktisk vejledningAf Kevin Beck | Opdateret 24. marts 2022 Hvad er isomerer? Isomerer er forbindelser, der deler den samme molekylære formel, men adskiller sig i struktur eller rumlig arrangement. De falder i to hov -
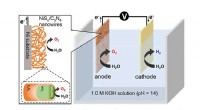 Et skridt nærmere en brintdrevet økonomi ved hjælp af en effektiv anode til vandopdelingSkematisk repræsentation af vanddissociationsprocessen ved lavt overpotentiale på ca. 32 mV ved anvendelse af NiS x nanotråde proppet ind i C 3 N 4 skede som anode til vandoxidation. Kredit:Niig
Et skridt nærmere en brintdrevet økonomi ved hjælp af en effektiv anode til vandopdelingSkematisk repræsentation af vanddissociationsprocessen ved lavt overpotentiale på ca. 32 mV ved anvendelse af NiS x nanotråde proppet ind i C 3 N 4 skede som anode til vandoxidation. Kredit:Niig
- Hvad er to af de måder, hvorpå en bil kan ændre en bil?
- Hvad sker der, når Jordens mantel trækker på bunden af techtoniske plader?
- Konvektion er overførslen af energi?
- Sekundære bygningsenheder (SBU'er) - vendepunktet i udviklingen af metal-organiske rammer (MOF'er…
- Teleforbindelse mellem det tropiske Stillehav og Antarktis
- Hvad er de vigtige obligatoriske problemer i fysik for STD 12.?


