At tælle alkanisomerer:en praktisk vejledning
Af Kevin Beck | Opdateret 24. marts 2022

Hvad er isomerer?
Isomerer er forbindelser, der deler den samme molekylære formel, men adskiller sig i struktur eller rumlig arrangement. De falder i to hovedkategorier:
- Stereoisomerer – molekyler med identiske tilslutningsmuligheder, men forskellige 3-D-orienteringer. Klassiske eksempler er D- og L-formerne af alanin, som er spejlbilleder, der ikke kan overlejres.
- Strukturelle isomerer - molekyler, hvis bindingssekvens er forskellig, hvilket giver helt forskellige forbindelser. Butan (C4 H10 ) og 2-methylpropan (C4 H10 ) illustrere dette; de er kemisk adskilte på trods af at de deler den samme formel.
Grenisomerer
I organisk kemi tillader kulstofs evne til at binde til andre kulstoffer kæder at forgrene sig. Disse grenisomerer er en undergruppe af strukturelle isomerer og har væsentlig indflydelse på fysiske og kemiske egenskaber. For store alkaner kan forgreningsmønstre blive ret komplekse.
Hvad er alkaner?
Alkaner er mættede kulbrinter, der udelukkende består af kulstof- og brintatomer forbundet med enkeltbindinger. Den generelle formel er Cn H2n+2 . Fordi hvert kulstof danner fire bindinger, tilbyder alkaner et stort landskab af isomere muligheder. Serien begynder med metan (CH4 ), ethan (C2 H6 ), og propan (C3 H8 ).
Nogle eksempler på isomertal:
- Butan (C4 H10 ) – 2 isomerer
- Pentan (C5 H12 ) – 3 isomerer
- Hexan (C6 H14 ) – 9 isomerer
- Dekan (C10 H22 ) – 75 isomerer
Der er ingen simpel formel i lukket form for antallet af alkanisomerer; i stedet konstruerer kemikere ofte repræsentative eksempler eller bruger beregningsværktøjer.
Isomer-kombinationsformelberegner
For at visualisere, hvordan en given formel kan arrangeres, kan du bruge en online isomergenerator. Prøv det interaktive værktøj her . Hvis du indtaster en formel, der ikke kan danne et stabilt molekyle, vil værktøjet med det samme indikere, at der ikke findes levedygtige isomerer.
At eksperimentere med umulige formler hjælper med at styrke de underliggende principper for valens og binding i organisk kemi.
 Varme artikler
Varme artikler
-
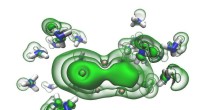 Et forsøg foreslået af en ph.d. elev kan omskrive kemi lærebøgerSolvatiserede elektroner (grønne) i hullerne mellem ammoniakmolekyler (blå og hvide) begynder at smelte sammen til et par, efterhånden som en opløsning bevæger sig mod at blive metallisk. Kredit:Ryan
Et forsøg foreslået af en ph.d. elev kan omskrive kemi lærebøgerSolvatiserede elektroner (grønne) i hullerne mellem ammoniakmolekyler (blå og hvide) begynder at smelte sammen til et par, efterhånden som en opløsning bevæger sig mod at blive metallisk. Kredit:Ryan -
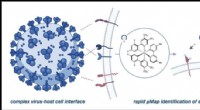 Forskere identificerer flere mulige indgangspunkter for COVID-spidsproteinVærtscelle- og virusgrænsefladen kan være kompleks og involvere mange proteiner, men µMap muliggør direkte undersøgelse af funktionelt vigtige interaktioner. Kredit:Saori Suzuki et al., Journal of the
Forskere identificerer flere mulige indgangspunkter for COVID-spidsproteinVærtscelle- og virusgrænsefladen kan være kompleks og involvere mange proteiner, men µMap muliggør direkte undersøgelse af funktionelt vigtige interaktioner. Kredit:Saori Suzuki et al., Journal of the -
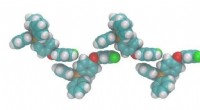 Subtile ion-interaktioner på molekylært niveau gør det muligt for forskere at indstille smeltepun…Simulering af et fluoreret salt, der viser kationjustering. Tilsætning af elektronegative fluoratomer (grønne) fører til justering med elektropositive fosforcentre (orange) i den faste fase, hvilket f
Subtile ion-interaktioner på molekylært niveau gør det muligt for forskere at indstille smeltepun…Simulering af et fluoreret salt, der viser kationjustering. Tilsætning af elektronegative fluoratomer (grønne) fører til justering med elektropositive fosforcentre (orange) i den faste fase, hvilket f -
 Gør renere, grønnere plast fra affaldsfiskdeleBrug af fiskeolie, forskere har lavet et polyurethan-lignende materiale. Kredit:Mikhailey Wheeler polyurethaner, en type plastik, er næsten overalt - i sko, tøj, køleskabe og byggematerialer. Men
Gør renere, grønnere plast fra affaldsfiskdeleBrug af fiskeolie, forskere har lavet et polyurethan-lignende materiale. Kredit:Mikhailey Wheeler polyurethaner, en type plastik, er næsten overalt - i sko, tøj, køleskabe og byggematerialer. Men


