Forskere identificerer flere mulige indgangspunkter for COVID-spidsprotein
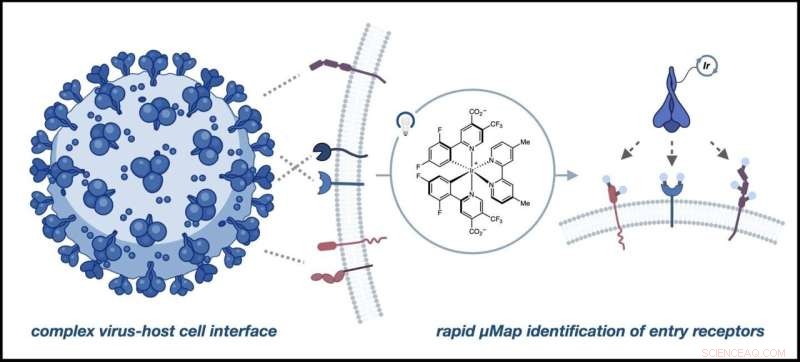
Værtscelle- og virusgrænsefladen kan være kompleks og involvere mange proteiner, men µMap muliggør direkte undersøgelse af funktionelt vigtige interaktioner. Kredit:Saori Suzuki et al., Journal of the American Chemical Society (2022). DOI:10.1021/jacs.2c06806
En af de væsentlige faktorer, som COVID-19-virussen har brug for for at trænge ind i en vært, er en receptor på en menneskelig celle - et sted, hvor det universelt anerkendte spikeprotein kan låse sig fast på celleoverfladen, gennembore det, fjerne dets smitsomme indhold og replikere.
Uden en receptor er der ingen replikation. Uden replikation er der ingen infektion.
Forskere ved Princeton University's Department of Chemistry og Department of Molecular Biology har brugt en cellulær kortlægningsteknologi kaldet µMap, som blev introduceret for blot to år siden af MacMillan Lab, til at afdække otte hidtil ukendte indgangspunkter af interesse for spikeproteinet.
Fire af dem, fandt forskerne, er funktionelt vigtige for viral indtræden.
Forskningen blev offentliggjort tidligere på måneden i Journal of the American Chemical Society (JACS) . Det kunne udvide rækken af værktøjer, der bruges til at bekæmpe virussen, især da den muterer og udvikler måder at undgå vacciner på.
Samarbejdsprojektet blev påbegyndt på højden af pandemisk usikkerhed for to år siden under Alexander Ploss, en førende virolog og professor i molekylærbiologi, og David MacMillan, James S. McDonnell Distinguished University Professor og en nobelprismodtager i kemi.
Forskere har vidst siden SARS-CoV-1-virusset dukkede op i 2003, at dens primære virale indgangsreceptor var et enzym kaldet angiotensin-konverterende enzym 2 eller ACE2. Dette enzym blev bekræftet i 2020 som den samme receptor for SARS-CoV-2, den virus, der forårsager COVID-19.
Men Princeton-projektet startede med den antagelse, at ACE2 ikke var den eneste historie.
"Vi vidste, at der er visse værtsmolekyler, som denne virus absolut afhænger af for at komme ind i lungeceller for at forårsage infektionen, og et af disse molekyler kaldes ACE2," sagde Ploss. "Så vi sagde grundlæggende, okay, lad os se, om der er mere derude. Vi ledte efter bindemidler med det samme.
"Men som du kan forestille dig, er indtrædensprocessen kompleks. Virusset binder sig til noget, og så skal det stadig passere gennem cellemembranen for at komme ind i en celle, og på den måde kan det interagere med andre værtsfaktorer. Det gør jeg' Jeg vil gerne sige, at alt er dikteret af viral indtræden. Det er klart, at der er en række lige så essentielle processer i cellen, efter at virussen er trængt ind, som kan påvirke sygdommens sværhedsgrad.
"Men det er åbenbart det første vigtige skridt. Hvis virussen ikke kan komme ind, er det slut."
Steve Knutson, en medforfatter på papiret og en postdoc-forsker i MacMillan Lab, tilføjede:"Mens opdagelsen af ACE2 som hovedreceptoren var en stor milepæl, fortæller den bestemt ikke hele historien om COVID-patologi. Biologi kan i sagens natur være promiskuøs, og vi gættede rigtigt, at SARS-CoV-2-spidsproteinet interagerer med flere værtscelleproteiner for at komme ind."
Han tilføjede, at undersøgelser som denne er en "perfekt" forskning, der passer til µMap-teknologien.
Spiket som µMap-antenne
Micromap (µMap) er en nærhedsmærkningsteknologi, der identificerer protein- og enzym-"naboer" på en celles overflade. Den bruger en fotokatalysator - et molekyle, der, når det aktiveres af lys, ansporer en kemisk reaktion - til at markere disse rumlige forhold ved at generere en markør, der mærker molekylære naboer.
I dette arbejde brugte forskere selve spidsproteinet som markør eller "antenne" til at mærke alle receptorsteder i nærheden af ACE2.
"Alex havde det store instinkt, at der er andre ting bortset fra ACE2, der kunne give dig mulighed for at tænke på smitteevne," sagde MacMillan. "Så det, vi gjorde, var at sætte denne fotokatalysator - og vi kalder dem antenner - på spidsproteinet, så hver gang det binder sig til ting på cellen i nærheden af ACE2, absorberer denne lille antenne den fotoniske energi, lyset.
"Men den kan ikke give den energi væk over lange afstande. Den kan kun give den til det, der er tæt på. Molekylet, der er frit svævende, skal dybest set støde på det inden for to nanometer," tilføjede MacMillan. "Så vi ved, hvad der er ved siden af det. Vi ved, hvad der interagerer med det."
Efter at teknologien identificerede otte nye receptorer, der interagerede med spikeproteinet, karakteriserede videnskabsmænd dem ved hjælp af en viruspseudopartikel. (En pseudopartikel efterligner viral indtrængen, men bærer ikke det genetiske materiale til at sprede virussen.) De isolerede derefter fire indgangsfaktorer, der var værd at undersøge nærmere.
"Pseudopartikelsystemet giver os mulighed for at afkoble viral optagelse og studere indgangsprocessen fra alt nedstrøms for den infektiøse cyklus," sagde Ploss. "Hvis du leder efter virkningen af visse værtsfaktorer på indtrængen, vil du gerne se, at du kan studere det uafhængigt af replikation. Så her introducerer vi grundlæggende et reportergen i cellen og kan derefter kvantificere, hvor effektivt indgang har fundet sted."
MacMillan sagde, at der var behov for yderligere arbejde for i sidste ende at bestemme receptorernes funktion, men forskerne spekulerer på, om de kan have et fingerpeg om sygdommens sværhedsgrad.
"Vi kan ikke sige, at alle otte faktorer er relateret til SARS-CoV-2-indgang," sagde Saori Suzuki, en associeret forsker i Ploss Lab. "Fire faktorer ud af otte var fremragende ved virologisk vurdering. Vi er nødt til at vurdere mere og evaluere mere præcist."
"I næste trin skal vi vurdere, hvordan disse faktorer understøtter ACE2 til virusindtrængning, og om nye virale varianter anvender det samme sæt af faktorer." + Udforsk yderligere
Coronavirus spike protein aktiveret naturligt immunrespons, beskadigede hjertemuskelceller
 Varme artikler
Varme artikler
-
 Sådan praktiseres beregninger for mikrodrop per minutTilvejebringelse af intravenøs (IV) væske er et væsentligt element i sygepleje, da et væld af medicin og andre stoffer gives på denne rute, især i ambulante hospitaler. IV-administration har fordelen
Sådan praktiseres beregninger for mikrodrop per minutTilvejebringelse af intravenøs (IV) væske er et væsentligt element i sygepleje, da et væld af medicin og andre stoffer gives på denne rute, især i ambulante hospitaler. IV-administration har fordelen -
 Metalkatalyserede reaktioner gjort enantioselektive ved brug af chiral kationKredit:University of Cambridge Forskere her har fundet frem til en strategi for at gøre en overgangsmetalkatalyseret kemisk reaktion enantioselektiv ved brug af en chiral kation. Arbejdet blev udf
Metalkatalyserede reaktioner gjort enantioselektive ved brug af chiral kationKredit:University of Cambridge Forskere her har fundet frem til en strategi for at gøre en overgangsmetalkatalyseret kemisk reaktion enantioselektiv ved brug af en chiral kation. Arbejdet blev udf -
 Bærbar biosensor advarer mod hjerteanfald og slagtilfældeDen bærbare måleenhed med USB -interface til tilslutning til bærbar computer. Softwaren installeret i bærbar computer giver GUI til at styre måleparametre og vise testresultaterne. Indsæt viser den em
Bærbar biosensor advarer mod hjerteanfald og slagtilfældeDen bærbare måleenhed med USB -interface til tilslutning til bærbar computer. Softwaren installeret i bærbar computer giver GUI til at styre måleparametre og vise testresultaterne. Indsæt viser den em -
 Forskere udvikler en ny Au-katalysator til hydroformyleringStrukturel modellering og ydelsessammenligning af Au-baserede katalysatorer. Kredit:SARI Som en af de største industrielle kemiske processer i dag, omdanner hydroformylering olefiner, H2 og CO ti
Forskere udvikler en ny Au-katalysator til hydroformyleringStrukturel modellering og ydelsessammenligning af Au-baserede katalysatorer. Kredit:SARI Som en af de største industrielle kemiske processer i dag, omdanner hydroformylering olefiner, H2 og CO ti


