Beregn pH-værdien af en 2M kaliumhydroxidopløsning:En trin-for-trin guide
Forstå begreberne
* KOH er en stærk base: Dette betyder, at det dissocierer fuldstændigt i vand og frigiver hydroxidioner (OH-) i opløsning.
* pH og pOH: pH måler surhedsgraden af en opløsning, mens pOH måler dens basicitet. De er forbundne med ligningen:pH + pOH =14
Beregninger
1. Find pOH:
* Da KOH er en stærk base, er koncentrationen af OH-ioner lig med koncentrationen af KOH.
* Derfor er [OH-] =2 M
* pOH =-log[OH-] =-log(2) ≈ -0,301
2. Beregn pH:
* pH + pOH =14
* pH =14 - pOH =14 - (-0,301) ≈ 14,301
Resultat
pH-værdien af en 2M kaliumhydroxidopløsning er ca. 14.301 . Dette indikerer en meget stærkt grundlæggende løsning.
Vigtig bemærkning:
* pH-skalaen er logaritmisk, hvilket betyder, at hver ændring i hele tal repræsenterer en tidobbel ændring i surhedsgrad eller basicitet.
* Håndter altid stærke baser med forsigtighed, da de kan forårsage alvorlige forbrændinger.
 Varme artikler
Varme artikler
-
 Molekylær lokkemad kan hjælpe hydrogeler med at hele sårHydrogeler udviklet ved Rice University inkorporerer tværbindere, der kan inkorporere bioaktive molekyler og hjælpe med at hele en række forskellige sår. Kredit:Jeff Fitlow/Rice University Ligesom
Molekylær lokkemad kan hjælpe hydrogeler med at hele sårHydrogeler udviklet ved Rice University inkorporerer tværbindere, der kan inkorporere bioaktive molekyler og hjælpe med at hele en række forskellige sår. Kredit:Jeff Fitlow/Rice University Ligesom -
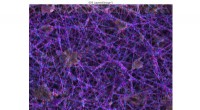 Forskningssamarbejde bringer nye koncepter for kalium-ion-batterierDette billede viser carbon nanofibre analyseret med en teknik kaldet energispredende røntgenspektroskopi efter at have gennemgået ladningsafladningscyklus i nye kaliumionbatterier. Batterierne er unde
Forskningssamarbejde bringer nye koncepter for kalium-ion-batterierDette billede viser carbon nanofibre analyseret med en teknik kaldet energispredende røntgenspektroskopi efter at have gennemgået ladningsafladningscyklus i nye kaliumionbatterier. Batterierne er unde -
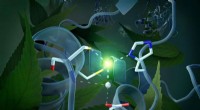 Universel reguleringsmekanisme i planteceller opdagetOmkring det katalytiske center er en gruppe molekyler, gating-domænet, som kan indtage to forskellige positioner. Kredit:M. Künsting / HZB Alle planteceller henter deres energi hovedsageligt fra t
Universel reguleringsmekanisme i planteceller opdagetOmkring det katalytiske center er en gruppe molekyler, gating-domænet, som kan indtage to forskellige positioner. Kredit:M. Künsting / HZB Alle planteceller henter deres energi hovedsageligt fra t -
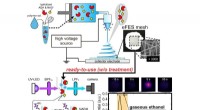 Bygning af bedre gasfasebiosensorer til bekæmpelse af sygdommeElektrospinningsenzymstrengen blev lavet med enzym- og coenzymholdig vandopløselig polymeropløsning (øverst). Det fremstillede elektrospinningsfluorometriske enzymstreng (eFES) mesh blev sat på fluore
Bygning af bedre gasfasebiosensorer til bekæmpelse af sygdommeElektrospinningsenzymstrengen blev lavet med enzym- og coenzymholdig vandopløselig polymeropløsning (øverst). Det fremstillede elektrospinningsfluorometriske enzymstreng (eFES) mesh blev sat på fluore
- Den største asteroide, der nærmer sig Jorden i 2022, vil zoome forbi vores planet i denne uge
- Hvad er bølgelængden på en hertz?
- Skelne mellem de subatomære partikler med hensyn til relativ ladning og masse?
- Hvordan er ild en ikke -levende ting i henhold til de 7 egenskaber?
- Alkalimetaller:Grundstoffer i den første kolonne i det periodiske system
- Navn 10 typer af encellede organismer?


