Konvertering af kobbersulfathydroxid:metoder og kemiske reaktioner
Her er en oversigt over muligheder, og hvordan du kan gribe dem an:
1. Transformation gennem kemiske reaktioner:
* Dehydrering: Kobber(II)sulfathydroxid (CuSO4·xCu(OH)2) kan dehydreres til dannelse af vandfrit kobber(II)sulfat (CuSO4). Dette gøres normalt ved at opvarme forbindelsen, hvilket driver vandmolekylerne væk. Den specifikke temperatur og tid, der kræves, vil afhænge af den nøjagtige form af din kobber(II)sulfathydroxid.
* Reaktion med syrer: Kobber(II)sulfathydroxid kan reagere med syrer og danne kobber(II)sulfat og vand. For eksempel:
* CuSO4·xCu(OH)2 + 2H2SO4 → (x+1)CuSO4 + (2x+1)H2O
* Reaktion med baser: Kobber(II)sulfathydroxid kan reagere med baser og danne kobber(II)hydroxid og et sulfatsalt. For eksempel:
* CuSO4·xCu(OH)2 + 2NaOH → (x+1)Cu(OH)2 + Na2SO4
2. Transformation gennem fysiske processer:
* Opløsning: Kobber(II)sulfathydroxid kan opløses i vand til dannelse af en opløsning af kobber(II)ioner (Cu²+) og sulfationer (SO₄²⁻).
* Krystallisering: Ved forsigtigt at fordampe vandet fra en kobber(II)sulfathydroxidopløsning, kan du krystallisere kobber(II)sulfat i forskellige former.
* Nedbør: Du kan bruge kemiske reaktioner til at udfælde kobber(II)sulfathydroxid fra en opløsning, hvilket potentielt ændrer dens form eller renhed.
3. Du tænker måske på noget andet:
* Cupric Sulfate Pentahydrate: Du kan være interesseret i at omdanne kobber(II)sulfatpentahydrat (CuSO₄·5H₂O), som er en almindelig form for kobber(II)sulfat. Dette kan dehydreres til vandfrit kobber(II)sulfat som beskrevet ovenfor.
For at få det mest nyttige svar, bedes du give flere oplysninger om, hvad du vil opnå:
* Hvad er startformen for dit kobber(II)sulfathydroxid?
* Hvad vil du opnå ved at transformere det? (f.eks. fremstille en specifik form, ændre dens kemiske sammensætning, øge renheden)
Når du har afklaret dit mål, kan jeg give mere specifikke instruktioner og vejledning om de relevante metoder.
 Varme artikler
Varme artikler
-
 Open source-software behandler hurtigt spektrale data, identificerer og kvantificerer lipidarter nø…LIQUID-grænsefladen. Kredit:Pacific Northwest National Laboratory Lipider spiller en nøglerolle i mange stofskiftesygdomme, herunder hypertension, diabetes, og slagtilfælde. Så det er vigtigt at h
Open source-software behandler hurtigt spektrale data, identificerer og kvantificerer lipidarter nø…LIQUID-grænsefladen. Kredit:Pacific Northwest National Laboratory Lipider spiller en nøglerolle i mange stofskiftesygdomme, herunder hypertension, diabetes, og slagtilfælde. Så det er vigtigt at h -
 Polaroids hjælper videnskabsmænd med at opdage farlig is på flyvemaskinerDer dannes is på en aluminiumsplade i et vejrkammer set med den fremgangsmåde, der er foreslået i undersøgelsen (venstre) og med det blotte øje (højre). Kredit:Viktor Grishaev et al./Cold Regions Scie
Polaroids hjælper videnskabsmænd med at opdage farlig is på flyvemaskinerDer dannes is på en aluminiumsplade i et vejrkammer set med den fremgangsmåde, der er foreslået i undersøgelsen (venstre) og med det blotte øje (højre). Kredit:Viktor Grishaev et al./Cold Regions Scie -
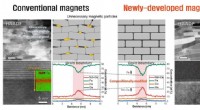 Udvikling af ny magnet, der reducerer brugen af sjældne jordarters grundstoffer med 30 %HAADF-STEM billeder og skematiske illustrationer af konventionelle magneter og nyudviklede magneter. Kredit:Korea Institute of Materials Science (KIMS) Et forskerhold ledet af Dr. Jung-Goo Lee og D
Udvikling af ny magnet, der reducerer brugen af sjældne jordarters grundstoffer med 30 %HAADF-STEM billeder og skematiske illustrationer af konventionelle magneter og nyudviklede magneter. Kredit:Korea Institute of Materials Science (KIMS) Et forskerhold ledet af Dr. Jung-Goo Lee og D -
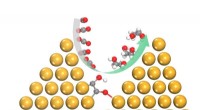 Super-selektive katalysatorer er nøglen til kulstofomdannelseDen unikke rumlige indeslutning induceret af kobbernanopyramider er afgørende for selektivt at generere ethylenglycol gennem en ny reaktionsvej. Kredit:Shizhang Qiao, Universitetet i Adelaide Kata
Super-selektive katalysatorer er nøglen til kulstofomdannelseDen unikke rumlige indeslutning induceret af kobbernanopyramider er afgørende for selektivt at generere ethylenglycol gennem en ny reaktionsvej. Kredit:Shizhang Qiao, Universitetet i Adelaide Kata
- Kan denne fyr hjælpe Intel med at fange AI-bølgen?
- Hvorfor betragtes denne hydroelektriske energikilde som en vedvarende ressource?
- Hvordan produceres kerneenergi kommercielt?
- Hvad er ikke-kommutative stoffer i kemi?
- Forskere viser, at silicium kan gengive fysiske fænomener, der udnyttes af avancerede telekommunika…
- Videnskabsprojekter om Newtons anden lov om bevægelse


