Iltladning:Forståelse af elektronegativitet og binding
* Atomer er neutrale: Atomer har lige mange protoner (positivt ladede) og elektroner (negativt ladede). Det betyder, at deres samlede ladning er nul.
* Elektronegativitet: Ilt er meget elektronegativt, hvilket betyder, at det har en stærk tendens til at tiltrække elektroner.
* Ionisk og kovalent binding: Ilt danner ofte kemiske bindinger med andre atomer. Disse bindinger kan være:
* Ionisk: Ilt kan få elektroner fra et andet atom, hvilket resulterer i en negativ ladning på oxygenatomet (en oxidion).
* Kovalent: Ilt kan dele elektroner med andre atomer. Mens det samlede molekyle er neutralt, kan oxygenatomet have en delvis negativ ladning, fordi det trækker de delte elektroner tættere på sig selv.
Opsummering:
* Iltatomer er neutrale i sig selv.
* Ilts høje elektronegativitet får det til at tiltrække elektroner i bindinger.
* Dette kan føre til, at oxygenatomer har en delvis negativ ladning i kovalente bindinger eller en fuld negativ ladning i ionbindinger.
Sidste artikelBeryllium Oxidationstal:Forståelse +2
Næste artikelVariabel valens i ioniske forbindelser:kobber og jern
 Varme artikler
Varme artikler
-
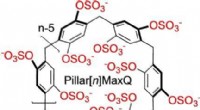 Molekylære beholdere til sekvestrering af neurotransmitterlægemidler i vandPillar[n]MaxQ:En ny værtsfamilie med høj affinitet til sekvestration i vand. Kredit:Angewandte Chemie International Edition Molekylære beholdere, der fjerner stoffer, toksiner, eller ildelugtende
Molekylære beholdere til sekvestrering af neurotransmitterlægemidler i vandPillar[n]MaxQ:En ny værtsfamilie med høj affinitet til sekvestration i vand. Kredit:Angewandte Chemie International Edition Molekylære beholdere, der fjerner stoffer, toksiner, eller ildelugtende -
 Leviterende proteiner kan hjælpe med at diagnosticere opioidmisbrug, andre sygdommeProteiner skabte specifikke former, når de blev leviteret, som et smiley ansigt af lag. Kredit:Michigan State University Forskere ved Michigan State Universitys Precision Health Program har hjulpe
Leviterende proteiner kan hjælpe med at diagnosticere opioidmisbrug, andre sygdommeProteiner skabte specifikke former, når de blev leviteret, som et smiley ansigt af lag. Kredit:Michigan State University Forskere ved Michigan State Universitys Precision Health Program har hjulpe -
 Superopløselig mikroskop afslører hemmeligheder ved dødbringende Nipah-virusKeng Chou (på bagsiden) og Qian Liu (forgrunden) forbereder sig på at observere en prøve ved hjælp af superopløsningsmikroskop udviklet af Chou og patenteret af UBC. Kredit:Lou Corpuz-Bosshart / UBC
Superopløselig mikroskop afslører hemmeligheder ved dødbringende Nipah-virusKeng Chou (på bagsiden) og Qian Liu (forgrunden) forbereder sig på at observere en prøve ved hjælp af superopløsningsmikroskop udviklet af Chou og patenteret af UBC. Kredit:Lou Corpuz-Bosshart / UBC -
 Stof fundet i fossile brændstoffer kan omdannes til ren diamantYu Lin viser modeller af diamantoider med en, to og tre bure, som kan forvandle sig til det indviklede, rent kulstofgitter af diamant – set i de større, blå model til højre – når den udsættes for ekst
Stof fundet i fossile brændstoffer kan omdannes til ren diamantYu Lin viser modeller af diamantoider med en, to og tre bure, som kan forvandle sig til det indviklede, rent kulstofgitter af diamant – set i de større, blå model til højre – når den udsættes for ekst
- Forskere bruger Piz Daint-simuleringer til at spore kraftig sommernedbør fra Middelhavet
- Dødelige californiske mudderskred viser behovet for kort og zoneinddeling, der bedre afspejler jord…
- Er klor et metalloid eller ikke-metal?
- Hvordan påvirker en DNA -base -deletion en organisme?
- Plantetilpasninger til liv på land:En omfattende oversigt
- Hvorfor ser vi den mørke side af månen?


