Hydrogen- og kulstofbinding:Hvorfor enkeltbindinger?
* Valenselektroner: Antallet af elektroner i et atoms yderste skal (valensskal) bestemmer, hvor mange bindinger det kan danne. Brint har kun én elektron i sin valensskal.
* Oktetregel: Atomer har tendens til at vinde, miste eller dele elektroner for at opnå en stabil konfiguration af otte valenselektroner (oktetreglen). Brint er dog en undtagelse. Den behøver kun to elektroner at opnå stabilitet.
* Obligationsdannelse: En enkeltbinding dannes, når to atomer deler et par elektroner. Da brint kun har én elektron at dele, kan det kun danne én enkeltbinding.
Derfor kan brint kun danne enkeltbindinger med andre atomer, inklusive kulstof.
Lad os overveje et eksempel:metan (CH4).
* Kulstof har fire valenselektroner og kan danne fire bindinger.
* Brint har én valenselektron og kan danne én binding.
De fire hydrogenatomer danner hver en enkelt binding med carbonatomet, hvilket resulterer i et stabilt molekyle af metan.
Dobbelt- og tredobbeltbindinger opstår mellem atomer, der har mere end én valenselektron at dele, f.eks. oxygen, nitrogen og selve kulstoffet.
 Varme artikler
Varme artikler
-
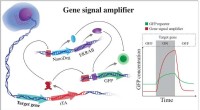 Stærke signaler viser, hvordan proteiner kommer og gårGensignalforstærkeren udviklet af bioscientists ved Rice University udmærker sig ved at detektere ekspressionen af målgener og kan også bruges til at detektere potentielt ethvert cellulært gen. Fors
Stærke signaler viser, hvordan proteiner kommer og gårGensignalforstærkeren udviklet af bioscientists ved Rice University udmærker sig ved at detektere ekspressionen af målgener og kan også bruges til at detektere potentielt ethvert cellulært gen. Fors -
 Springende og holdbare gummibelægninger kan redde tusinder af liv, siger forskereKredit:Astrid Gast, Shutterstock Et team af forskere støttet af et EU -initiativ tester belægninger lavet af genbrugsdæk for at forhindre skader som følge af ulykker og fald. Fald og faldrelatere
Springende og holdbare gummibelægninger kan redde tusinder af liv, siger forskereKredit:Astrid Gast, Shutterstock Et team af forskere støttet af et EU -initiativ tester belægninger lavet af genbrugsdæk for at forhindre skader som følge af ulykker og fald. Fald og faldrelatere -
 Behov for strenge procedurer inden for elektrokemisk produktion af ammoniakElektrokemisk fremstillet ammoniak. Kredit:Jakob Kibsgaard Ammoniak (NH 3 ) er et af de mest udbredte kemikalier, med en global produktion på 170 megaton om året. Det er nøgleingrediensen i prod
Behov for strenge procedurer inden for elektrokemisk produktion af ammoniakElektrokemisk fremstillet ammoniak. Kredit:Jakob Kibsgaard Ammoniak (NH 3 ) er et af de mest udbredte kemikalier, med en global produktion på 170 megaton om året. Det er nøgleingrediensen i prod -
 To-trins gassensor rapporterer om jordens dynamikEn robust to-trins mikrobiel sensor udviklet ved Rice University vil hjælpe forskere med at observere genekspression og biotilgængelighed af næringsstoffer i miljøer som jord og sedimenter uden at for
To-trins gassensor rapporterer om jordens dynamikEn robust to-trins mikrobiel sensor udviklet ved Rice University vil hjælpe forskere med at observere genekspression og biotilgængelighed af næringsstoffer i miljøer som jord og sedimenter uden at for
- Maskindetektering af menneske-objekt-interaktion i billeder og videoer
- Hvorfor vira er vanskelige at klassificere som levende organismer?
- Hvad er fromulaen for kinetisk energi?
- Hvad er fordelen ved phosphoryleringskaskade?
- Sådan fungerer CO2 -skrubning
- Mindre liv:Begrænset genanvendelse af fosfor undertrykte jordens tidlige biosfære


