Natrium vs. Magnesium:Forståelse af ioniseringsenergiforskelle
Forståelse af ioniseringsenergi
Ioniseringsenergi er den mindste mængde energi, der kræves for at fjerne en elektron fra et gasformigt atom i dets elektroniske jordtilstand.
Elektronkonfiguration og afskærmning
* Natrium (Na): [Ne] 3s¹
* Magnesium (Mg): [Ne] 3s²
Natrium har en elektron i sin yderste skal (3s¹), mens magnesium har to (3s²). Denne enlige elektron i natrium er længere væk fra kernen og oplever mindre effektiv nuklear ladning (den netto positive ladning oplevet af en elektron) på grund af den afskærmende effekt af de indre elektroner.
Effektiv nuklear ladning
Den effektive kerneladning er svagere for natrium, fordi den enkelte elektron i 3s orbitalen er afskærmet fra kernen af de indre elektroner (dem i [Ne]-kernen). I magnesium oplever de to 3s elektroner en stærkere effektiv nuklear ladning, fordi de begge er afskærmet i samme grad af de indre elektroner.
Nøglepunkter
* Nemmere at fjerne: Den svagere effektive kerneladning i natrium betyder, at dens yderste elektron er mindre tæt bundet til kernen. Derfor kræver det mindre energi at fjerne denne elektron, hvilket resulterer i en lavere ioniseringsenergi.
* Sværere at fjerne: I magnesium betyder den stærkere effektive nukleare ladning, at elektronerne er tættere bundet til kernen, hvilket fører til en højere ioniseringsenergi.
Opsummering: Den lavere ioniseringsenergi af natrium sammenlignet med magnesium skyldes primært forskellen i effektiv kerneladning, som de yderste elektroner oplever. Natriums enkelt yderste elektron fjernes lettere, fordi den oplever mindre tiltrækning til kernen.
Sidste artikelBrint i metallurgi:applikationer og reduktionsprocesser
Næste artikelHvad er råolieforbindelser? Forståelse af kulbrinter
 Varme artikler
Varme artikler
-
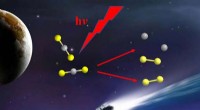 Dalian Coherent Light Source afslører oprindelsen af interstellar disulfurForskere observerede direkte C + S2-kanalen i CS 2 fotodissociation. Kredit:LI Zhenxing At studere skabelsen og udviklingen af svovlholdige forbindelser i det ydre rum er afgørende for at fors
Dalian Coherent Light Source afslører oprindelsen af interstellar disulfurForskere observerede direkte C + S2-kanalen i CS 2 fotodissociation. Kredit:LI Zhenxing At studere skabelsen og udviklingen af svovlholdige forbindelser i det ydre rum er afgørende for at fors -
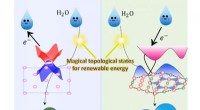 Fremskynde brintproduktionen ved hjælp af de magiske topologiske overfladetilstandeTopologiske ikke-trivielle overfladetilstande kan acceptere eller donere elektroner under vandelektrolyseprocessen. Kredit:MPI CPfS Brintøkonomien anses for at være en af de bedste muligheder fo
Fremskynde brintproduktionen ved hjælp af de magiske topologiske overfladetilstandeTopologiske ikke-trivielle overfladetilstande kan acceptere eller donere elektroner under vandelektrolyseprocessen. Kredit:MPI CPfS Brintøkonomien anses for at være en af de bedste muligheder fo -
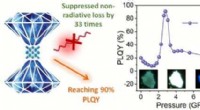 Opnå 90% PL-kvanteudbytte i 1-D metalhalogenid ved trykundertrykt ikke-strålende tabKredit:Center for High Pressure Science &Technology Advanced Research Lavdimensionelle perovskit-relaterede metalhalogenider er opstået som en ny klasse af lysemitterende materialer med afstemt br
Opnå 90% PL-kvanteudbytte i 1-D metalhalogenid ved trykundertrykt ikke-strålende tabKredit:Center for High Pressure Science &Technology Advanced Research Lavdimensionelle perovskit-relaterede metalhalogenider er opstået som en ny klasse af lysemitterende materialer med afstemt br -
 Forskere finder en sammenhæng mellem kræft og aldring inde i vores cellerHollings Cancer Center-forsker Besim Ogretmen er SmartState Endowed Chair i Lipidomics and Drug Discovery ved Medical University of South Carolina. Kredit:Brennan Wesley Forskere ved Hollings Canc
Forskere finder en sammenhæng mellem kræft og aldring inde i vores cellerHollings Cancer Center-forsker Besim Ogretmen er SmartState Endowed Chair i Lipidomics and Drug Discovery ved Medical University of South Carolina. Kredit:Brennan Wesley Forskere ved Hollings Canc
- Hvor smarte er spækhuggere? Spækhuggere har den næststørste hjerne af alle havpattedyr
- Hvad kan få cellecyklussen til at blive ukontrolleret?
- Den kontrollerende organelle i en celle er?
- Hvad er formeltemperaturen?
- Er Nepal og Florida på den samme breddegrad?
- Hvilken cellestruktur indeholder kromosomerne?


