Beregning af pH af en KOH-opløsning:En trin-for-trin guide
Forstå begreberne
* KOH er en stærk base: Det betyder, at det dissocierer fuldstændigt i vand og frigiver alle dets hydroxidioner (OH-).
* pH og pOH: pH og pOH er relateret til koncentrationen af henholdsvis hydrogenioner (H+) og hydroxidioner (OH-). De er forbundet med ligningen:pH + pOH =14.
Beregninger
1. Find pOH: Da KOH er en stærk base, er koncentrationen af OH-ioner lig med koncentrationen af KOH-opløsningen.
* [OH-] =1 x 10^-5 M
* pOH =-log[OH-] =-log(1 x 10^-5) =5
2. Beregn pH:
* pH + pOH =14
* pH =14 - pOH =14 - 5 =9
Svar: pH-værdien af en 1 x 10^-5 M KOH-opløsning er 9 .
 Varme artikler
Varme artikler
-
 Nye potente analoger af plantehormon giver tørkestresslindring for afgrøderBlandt abiotisk stress, tørkestress er en af de vigtigste kilder til tab af afgrøder over hele kloden. En beskyttelsesstrategi er udvikling af kemikalier, der hjælper afgrøder med at klare vandmange
Nye potente analoger af plantehormon giver tørkestresslindring for afgrøderBlandt abiotisk stress, tørkestress er en af de vigtigste kilder til tab af afgrøder over hele kloden. En beskyttelsesstrategi er udvikling af kemikalier, der hjælper afgrøder med at klare vandmange -
 Polymer tvilling:Nyt implantat efterligner knoglestrukturImplantat, forberedt til kompressionstest. Kredit:Sergey Gnuskov/NUST MISIS Forskere fra National University of Science and Technology (MISIS) udviklede et unikt hybrid knogleimplantat, hvis kerne
Polymer tvilling:Nyt implantat efterligner knoglestrukturImplantat, forberedt til kompressionstest. Kredit:Sergey Gnuskov/NUST MISIS Forskere fra National University of Science and Technology (MISIS) udviklede et unikt hybrid knogleimplantat, hvis kerne -
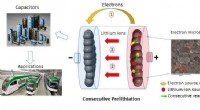 Mod en billig industrialisering af lithium-ion kondensatorerFortløbende forbehandling med to tilsætningsstoffer (pyren i gult og Li3PO4 i rødt). Den kemiske analyse, der anvendes i elektronmikroskopibilledet, gør det muligt at lokalisere Li3PO4 (røde områder).
Mod en billig industrialisering af lithium-ion kondensatorerFortløbende forbehandling med to tilsætningsstoffer (pyren i gult og Li3PO4 i rødt). Den kemiske analyse, der anvendes i elektronmikroskopibilledet, gør det muligt at lokalisere Li3PO4 (røde områder). -
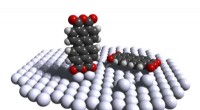 Tricky feat med stand-up molekyleOprejst PTCDA -molekyle på en sølvplatform (til venstre); normalt aflejres molekylet fladt mod det flade lag af sølvatomer (til højre). Kredit:Forschungszentrum Jülich / T. Esat I de seneste årtie
Tricky feat med stand-up molekyleOprejst PTCDA -molekyle på en sølvplatform (til venstre); normalt aflejres molekylet fladt mod det flade lag af sølvatomer (til højre). Kredit:Forschungszentrum Jülich / T. Esat I de seneste årtie
- Hvad er molekylvægt af Haucl4?
- Hvad er geomorfisk kraft?
- vulkansk aktivitet, faldende havilt udløste masseudryddelse af gamle organismer
- Hvad er en række kemiske reaktioner, der producerer sukker fra kuldioxid?
- Hvor potentiel energi opstår en elastisk fjeder?
- Skriv NaCl Plus AGC2H3O2 er lig med NAC2H3O2 AgCl som en nettoionisk ligning?


