Alkalimetaller vs. overgangsmetaller:Reaktivitet forklaret
* Elektronkonfiguration: Alkalimetaller har kun én valenselektron (i den yderste skal), som de let taber for at opnå en stabil oktet. Dette gør dem meget reaktive. Overgangsmetaller har på den anden side multiple valenselektroner og kan miste forskellige antal elektroner, hvilket gør deres reaktivitet mere kompleks.
* Elektropositivitet: Alkalimetaller er meget elektropositive, hvilket betyder, at de har en stærk tendens til at miste elektroner og danne positive ioner. Dette gør, at de let reagerer med andre elementer, især ikke-metaller. Overgangsmetaller er mindre elektropositive og danner mindre let ioner.
* Ioniseringsenergi: Alkalimetaller har lavere ioniseringsenergi sammenlignet med overgangsmetaller. Det betyder, at det tager mindre energi at fjerne en elektron fra et alkalimetalatom, hvilket gør dem mere reaktive.
Undtagelser:
Selvom den generelle tendens holder stik, er der nogle undtagelser. For eksempel er nogle overgangsmetaller som guld og platin meget ureaktive på grund af deres høje ioniseringsenergier og tilstedeværelsen af fyldte d-orbitaler.
Opsummering:
Selvom der er nogle undtagelser, er alkalimetaller generelt mere reaktive end overgangsmetaller på grund af deres elektronkonfigurationer, elektropositivitet og lavere ioniseringsenergier.
 Varme artikler
Varme artikler
-
 Effektive måder at smelte is på uden varmeAf Jason Gabriel • Opdateret 24. marts 2022 Vand bliver til is ved 32°F (0°C). Selvom opvarmning er den mest ligetil måde at smelte is på, er det ikke altid muligt - især i kolde klimaer, eller når e
Effektive måder at smelte is på uden varmeAf Jason Gabriel • Opdateret 24. marts 2022 Vand bliver til is ved 32°F (0°C). Selvom opvarmning er den mest ligetil måde at smelte is på, er det ikke altid muligt - især i kolde klimaer, eller når e -
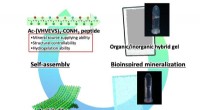 Bioinspireret mineralisering af calciumcarbonat i peptidhydrogelBioinspireret mineralisering. Kredit:Kazuki Murai et al., Journal of Asian Ceramic Societies, Taylor og Francis Et team af forskere har udviklet en biomimetisk mineralisering af calciumcarbonat ve
Bioinspireret mineralisering af calciumcarbonat i peptidhydrogelBioinspireret mineralisering. Kredit:Kazuki Murai et al., Journal of Asian Ceramic Societies, Taylor og Francis Et team af forskere har udviklet en biomimetisk mineralisering af calciumcarbonat ve -
 Upcycling-processen bringer nyt liv til gamle jeansKredit:American Chemical Society En voksende befolkning, stigende levestandard og hurtigt skiftende mode sender hvert år bjerge af tøjaffald til verdens lossepladser. Selvom der findes processer t
Upcycling-processen bringer nyt liv til gamle jeansKredit:American Chemical Society En voksende befolkning, stigende levestandard og hurtigt skiftende mode sender hvert år bjerge af tøjaffald til verdens lossepladser. Selvom der findes processer t -
 Er opvaskemaskinekapsler sikre? Videnskaben bag PVA og miljøpåvirkningYanchuk Viktoriia/Shutterstock Opvaskemaskine bælg forenkler en kedelig opgave, men deres klare film har udløst bekymringer om plastikforurening og sundhedsrisici. Filmen er lavet af polyvinylalkohol
Er opvaskemaskinekapsler sikre? Videnskaben bag PVA og miljøpåvirkningYanchuk Viktoriia/Shutterstock Opvaskemaskine bælg forenkler en kedelig opgave, men deres klare film har udløst bekymringer om plastikforurening og sundhedsrisici. Filmen er lavet af polyvinylalkohol
- Gener, DNA og kromosomer:Forståelse af forholdet
- Hvor mange stjerner er der i en supercluster?
- Hvad er tyngdekraftsassist?
- E. coli aktiv transport:kalium og hypertoniske løsninger
- Når stjerner løber tør for brændstof, kollapser det på sig selv og bliver hvad?
- En historie om syrer og alkalier:Hvem opdagede dem først?


