Jernholdig vs. ikke-jernholdig metalkorrosion:Forstå forskellene
Korrosion af jernholdige vs. ikke-jernholdige metaller:et sammenbrud
Mens både jernholdige og ikke-jernholdige metaller kan korrodere, er mekanismerne og produkterne af korrosion betydeligt forskellige. Her er en oversigt:
Jernholdige metaller (jernbaserede)
* Mekanisme: Primært elektrokemisk korrosion . Dette involverer dannelsen af en elektrokemisk celle, hvor jern fungerer som anode, taber elektroner og oxiderer for at danne jernioner (Fe²⁺). Elektronerne strømmer til katoden, typisk et mindre ædelmetal eller en anden del af jernoverfladen, hvor de reducerer ilt fra miljøet til dannelse af hydroxidioner (OH⁻). Disse ioner reagerer derefter med jernioner og danner rust (Fe₂O₃·xH2O), et hydreret jernoxid.
* Produkter: Rust, en rødbrun, flaget oxid, der er porøs og tillader yderligere korrosion at forekomme.
* Faktorer, der påvirker korrosion:
* Tilstedeværelse af fugt: Rustdannelse kræver vand og ilt.
* Elektrolyt: Tilstedeværelsen af salte, syrer eller andre elektrolytter fremskynder den elektrokemiske proces.
* Stress: Mekanisk stress kan øge korrosionshastigheden.
* Temperatur: Højere temperaturer øger generelt korrosionshastigheden.
* pH: Miljøets pH kan påvirke hastigheden og typen af korrosion.
* Beskyttelse:
* Belægninger: Maling, emaljer og galvanisering (belægning med zink) kan forhindre fugt og ilt i at nå metaloverfladen.
* Legering: Tilføjelse af elementer som krom, nikkel og molybdæn til jern kan skabe korrosionsbestandigt rustfrit stål.
* Katodisk beskyttelse: Brug af et mere aktivt metal (f.eks. zink) til at ofre sig selv og beskytte det jernholdige metal.
Ikke-jernholdige metaller
* Mekanisme: Varierer afhængigt af det specifikke metal. Nogle almindelige typer omfatter:
* Oxidation: Dannelse af oxider på metaloverfladen (f.eks. aluminiumoxid).
* Sulfidering: Reaktion med svovlforbindelser til dannelse af sulfider (f.eks. kobbersulfid).
* Klorering: Reaktion med chlorforbindelser til dannelse af chlorider (f.eks. sølvchlorid).
* Produkter: Varierer afhængigt af metal og korrosionsproces.
* Faktorer, der påvirker korrosion:
* Miljø: Tilstedeværelsen af specifikke elementer som svovl, klor eller oxygen kan fremskynde korrosion.
* Temperatur: Højere temperaturer øger generelt korrosionshastigheden.
* pH: Miljøets pH kan påvirke hastigheden og typen af korrosion.
* Beskyttelse:
* Belægninger: I lighed med jernholdige metaller kan belægninger beskytte mod miljøfaktorer.
* Legering: Tilføjelse af elementer kan forbedre korrosionsbestandigheden af ikke-jernholdige metaller.
* Anodisk beskyttelse: Påføring af en kontrolleret elektrisk strøm til metaloverfladen for at undertrykke korrosion.
Nøgleforskelle:
* Korrosionsprodukt: Rust i jernholdige metaller er porøs og tillader yderligere korrosion, mens oxidlag på nogle ikke-jernholdige metaller kan fungere som beskyttende barrierer.
* Mekanisme: Jernholdige metaller korroderer primært gennem elektrokemiske processer, mens ikke-jernholdige metaller kan have forskellige korrosionsmekanismer afhængigt af metallet og miljøet.
* Beskyttelsesmetoder: Nogle beskyttelsesmetoder, som galvanisering, er specifikke for jernholdige metaller, mens andre, som anodisk beskyttelse, bruges til ikke-jernholdige metaller.
Opsummering: Mens både jernholdige og ikke-jernholdige metaller kan korrodere, adskiller deres korrosionsmekanismer, produkter og beskyttelsesmetoder sig væsentligt på grund af de unikke kemiske egenskaber af hvert metal. At forstå disse forskelle er afgørende for at vælge passende materialer og beskyttelsesmetoder til forskellige anvendelser.
 Varme artikler
Varme artikler
-
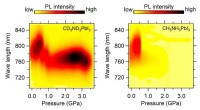 Jo tungere, jo bedre - overlegen stabilitet i isotopfunktionaliserede perovskitterFarveplot af de trykafhængige PL-udviklinger af CD3ND3PbI3 (venstre) og CH3NH3PbI3 (højre) enkeltkrystaller. Kredit:Gang Liu Organisk-uorganisk hybrid blyiodidperovskiter er universelt anerkendt s
Jo tungere, jo bedre - overlegen stabilitet i isotopfunktionaliserede perovskitterFarveplot af de trykafhængige PL-udviklinger af CD3ND3PbI3 (venstre) og CH3NH3PbI3 (højre) enkeltkrystaller. Kredit:Gang Liu Organisk-uorganisk hybrid blyiodidperovskiter er universelt anerkendt s -
 At overliste patogener – forskning har til formål at løse centrale vandfiltreringsudfordringerKredit:Texas A&M University I år 2025 forventes det, at næsten 2 milliarder mennesker vil bo i områder med knaphed på vand. Disse fremskrivninger peger på behovet for avancerede vand- og spildevan
At overliste patogener – forskning har til formål at løse centrale vandfiltreringsudfordringerKredit:Texas A&M University I år 2025 forventes det, at næsten 2 milliarder mennesker vil bo i områder med knaphed på vand. Disse fremskrivninger peger på behovet for avancerede vand- og spildevan -
 Sådan neutraliseres saltsyre sikkert med bagepulverAf Louis Gutierrez Opdateret 30. august 2022 eskaylim/iStock/GettyImages Bagepulver, eller natriumbicarbonat, er en mild base, der effektivt neutraliserer syrer, herunder den stærke saltsyre (HCl).
Sådan neutraliseres saltsyre sikkert med bagepulverAf Louis Gutierrez Opdateret 30. august 2022 eskaylim/iStock/GettyImages Bagepulver, eller natriumbicarbonat, er en mild base, der effektivt neutraliserer syrer, herunder den stærke saltsyre (HCl). -
 Fysikere forklarer, hvordan store sfæriske vira dannesSiyu Li (til venstre) er kandidatstuderende i laboratoriet hos Roya Zandi, en professor i fysik ved UC Riverside. De ses her holde forskellige icosahedral strukturer. Kredit:I. Pittalwala, UC Riversid
Fysikere forklarer, hvordan store sfæriske vira dannesSiyu Li (til venstre) er kandidatstuderende i laboratoriet hos Roya Zandi, en professor i fysik ved UC Riverside. De ses her holde forskellige icosahedral strukturer. Kredit:I. Pittalwala, UC Riversid
- Hvordan passerer andre molekyler gennem den selektivt permeable cellemembran?
- Hvorfor er bjerge køligere, hvis de nærmer sig solen?
- Hvordan konverterer du 4,50 til videnskabelig notation?
- Udfordrende perspektiver på magmakamre med nye fund
- Kvantepunkter giver kvantitativ profil af kræft i bugspytkirtelkræft på enkeltceller
- Hvorfor er Jorden så smuk?


