Enkelt-erstatningsreaktioner:Fælles miljøer og nøglefaktorer
Her er hvorfor:
* Ioniske forbindelser: Enkelt-erstatningsreaktioner involverer typisk ioniske forbindelser opløst i vand, hvor ionerne er frie til at bevæge sig og interagere.
* Reaktivitetsserie: Reaktiviteten af metaller (eller ikke-metaller) spiller en afgørende rolle. Et mere reaktivt grundstof kan fortrænge et mindre reaktivt grundstof fra dets forbindelse i opløsning.
* Elektrokemiske processer: Reaktionen involverer ofte overførsel af elektroner, hvilket gør det til en elektrokemisk proces.
Eksempler:
* Reaktion af zink med kobber(II)sulfatopløsning:
```
Zn(s) + CuSO4(aq) → ZnSO4(aq) + Cu(s)
```
Her er zink mere reaktivt end kobber, så det fortrænger kobber fra opløsningen.
* Reaktion af klorgas med kaliumbromidopløsning:
```
Cl2(g) + 2KBr(aq) → 2KCl(aq) + Br2(l)
```
Klor er mere reaktivt end brom, så det fortrænger brom fra opløsningen.
Mens vandige opløsninger er det mest almindelige miljø, kan enkeltudskiftningsreaktioner også forekomme i andre miljøer, såsom:
* Smeltede salte: Der kan forekomme reaktioner mellem smeltede metaller og smeltede salte.
* Gasformige blandinger: Reaktioner kan forekomme mellem reaktive gasser, såsom reaktionen af brint med klor til dannelse af hydrogenchlorid.
Imidlertid giver vandige opløsninger de ideelle betingelser for mange enkelt-erstatningsreaktioner på grund af tilstedeværelsen af opløste ioner og evnen for reaktionerne til at forløbe via elektrokemiske processer.
 Varme artikler
Varme artikler
-
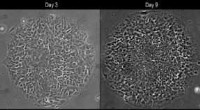 Mod en stamcellemodel for udvikling af menneskeligt nervesystemSkiveformede kolonier vist med fasekontrast (øverst) og fluorescens (nederst) mikroskopi. Mellem dag 3 og dag 9, celler i midten af kolonien vokser hurtigere og bliver meget tættere pakket. Begrænse
Mod en stamcellemodel for udvikling af menneskeligt nervesystemSkiveformede kolonier vist med fasekontrast (øverst) og fluorescens (nederst) mikroskopi. Mellem dag 3 og dag 9, celler i midten af kolonien vokser hurtigere og bliver meget tættere pakket. Begrænse -
 Ny opdagelse gør hurtigopladning, bedre ydende lithium-ion-batterier muligtMaterialeforskning -- udgivet i Naturkommunikation -- muliggør lithium-ion-batterier, der kan oplades i løbet af få minutter, men som stadig fungerer med høj kapacitet. Kredit:Rensselaer Polyteknisk
Ny opdagelse gør hurtigopladning, bedre ydende lithium-ion-batterier muligtMaterialeforskning -- udgivet i Naturkommunikation -- muliggør lithium-ion-batterier, der kan oplades i løbet af få minutter, men som stadig fungerer med høj kapacitet. Kredit:Rensselaer Polyteknisk -
 Ny katalysator gør styrenfremstilling billigere, grønnereKredit:North Carolina State University Kemiingeniørforskere har udviklet en ny katalysator, der markant øger udbyttet i styrenfremstilling, samtidig med at energiforbruget og drivhusgasemissionern
Ny katalysator gør styrenfremstilling billigere, grønnereKredit:North Carolina State University Kemiingeniørforskere har udviklet en ny katalysator, der markant øger udbyttet i styrenfremstilling, samtidig med at energiforbruget og drivhusgasemissionern -
 Video:Hvorfor limejuice brænder din hud i solenKredit:The American Chemical Society Vidste du, at det at lave margaritas og derefter tage til stranden kan give dig en smertefuld, hævelse brænde? I denne episode af Reaktioner, vi chatter med k
Video:Hvorfor limejuice brænder din hud i solenKredit:The American Chemical Society Vidste du, at det at lave margaritas og derefter tage til stranden kan give dig en smertefuld, hævelse brænde? I denne episode af Reaktioner, vi chatter med k
- Billede:Fenix prototype - en lille, satellitforstærker i pen
- Hvilket kontinent har den lavest registrerede temperatur på jorden?
- Hvor startede Pathfinder Space -sonden fra?
- Hvilke emner studerer videnskabsmand?
- Hvad hedder processen, når en celle omgiver stor partikel med pseudopodia og derefter opsuger den?
- Hvordan immunresponsen bidrager til Homeostasis


