Benzen:hvorfor det er klassificeret som en umættet forbindelse | Kemi forklaret
1. Brintmangel:
* Teoretisk mætning: Et fuldt mættet carbonhydrid med seks carbonatomer ville have formlen C6 H14 (efter den generelle formel Cn H2n+2 ).
* Benzens formel: Benzen har formlen C6 H6 , hvilket betyder, at den har fire færre brintatomer end en mættet forbindelse med seks carbonatomer. Denne "brintmangel" er et kendetegn for umættethed.
2. Reaktivitet:
* Tilføjelsesreaktioner: I modsætning til mættede kulbrinter (alkaner), som er relativt ureaktive, gennemgår benzen *substitutionsreaktioner*, hvor et brintatom erstattes af et andet atom eller en anden gruppe. Dette skyldes, at elektronerne i dets ringsystem er delokaliserede og mere stabile end en typisk dobbeltbinding.
* Hydrogenering: Benzen kan tvinges til at gennemgå hydrogenering, tilføje brintatomer til ringen og bryde det delokaliserede system. Dette kræver betydelig energi og tryk, hvilket yderligere indikerer dets umættede natur.
3. Molekylær struktur:
* Delokaliserede elektroner: De seks elektroner i ringen er ikke lokaliseret mellem specifikke carbonatomer som typiske dobbeltbindinger. I stedet bliver de delokaliseret og danner en sky over og under ringens plan. Denne delokalisering bidrager til dens stabilitet, men indikerer også tilgængeligheden af elektroner til reaktioner.
4. Spektroskopiske beviser:
* NMR-spektroskopi: De kemiske skift af hydrogenatomerne i benzen er karakteristiske for en aromatisk ring, hvilket indikerer delokalisering af elektroner.
* UV-Vis-spektroskopi: Benzen absorberer ultraviolet lys på grund af de delokaliserede pi-elektroner, hvilket er en anden indikation af dens umættede natur.
Opsummering: Mens benzens struktur ikke viser traditionelle dobbeltbindinger, bekræfter dens brintmangel, reaktivitet, delokaliserede elektroner og spektroskopiske egenskaber alle, at det er en umættet forbindelse. Udtrykket "aromatisk" bruges til at beskrive denne unikke type umættethed.
 Varme artikler
Varme artikler
-
 Miljøvenlige kemikalier kan faktisk forbedre mineralforarbejdningenKobbermineral koncentreret efter flotation. Kredit:Aalto University / Nina Pulkkis Metaller udvundet fra jordskorpen er afgørende for vores daglige produkter, men deres produktion lægger en tung b
Miljøvenlige kemikalier kan faktisk forbedre mineralforarbejdningenKobbermineral koncentreret efter flotation. Kredit:Aalto University / Nina Pulkkis Metaller udvundet fra jordskorpen er afgørende for vores daglige produkter, men deres produktion lægger en tung b -
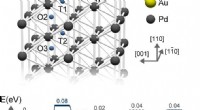 Hvorfor guld-palladium-legeringer er bedre end palladium til brintlagringAu-atomerne destabiliserer kemisorberet brint, dermed øge deres energi og reducere barrieren. Kredit:2018 Shohei Ogura, Institut for Industrividenskab, Universitetet i Tokyo Materialer, der absorb
Hvorfor guld-palladium-legeringer er bedre end palladium til brintlagringAu-atomerne destabiliserer kemisorberet brint, dermed øge deres energi og reducere barrieren. Kredit:2018 Shohei Ogura, Institut for Industrividenskab, Universitetet i Tokyo Materialer, der absorb -
 Ammoniakdissociation i vandig opløsning:reaktionsligningenNår et opløst stof opløses i vand, kan det simpelthen dissociere i dets bestanddele eller reagere med opløsningsmidlet. Natriumchlorid, for eksempel, ioniserer til Na⁺ og Cl⁻ uden at ændre vandmolekyl
Ammoniakdissociation i vandig opløsning:reaktionsligningenNår et opløst stof opløses i vand, kan det simpelthen dissociere i dets bestanddele eller reagere med opløsningsmidlet. Natriumchlorid, for eksempel, ioniserer til Na⁺ og Cl⁻ uden at ændre vandmolekyl -
 Forskere udvikler mere effektivt katalytisk materiale til brændselscelle applikationerDette billede i høj opløsning viser fordelingen af platin og zinkatomer i en PtZn intermetallisk nanopartikel. Kredit:Ames Laboratory, Det amerikanske energiministerium Forskere ved Ames Laborat
Forskere udvikler mere effektivt katalytisk materiale til brændselscelle applikationerDette billede i høj opløsning viser fordelingen af platin og zinkatomer i en PtZn intermetallisk nanopartikel. Kredit:Ames Laboratory, Det amerikanske energiministerium Forskere ved Ames Laborat
- Hvorfor er der vind på Mars?
- USA i dybfrysning, mens meget af verden er ekstra toasty? Endnu en gang er det klimaforandringer
- Hvor mange ounces er der i en fane af smør?
- Glas med omskiftelig opacitet kan forbedre solceller og lysdioder
- Hvor er biome placeret?
- Hvad hedder det naturlige miljø for levende organisme?


