Ammoniakdissociation i vandig opløsning:reaktionsligningen
Når et opløst stof opløses i vand, kan det simpelthen dissociere i dets bestanddele eller reagere med opløsningsmidlet. Natriumchlorid, for eksempel, ioniserer til Na⁺ og Cl⁻ uden at ændre vandmolekylerne. Ammoniak opfører sig anderledes:Som base accepterer den en proton fra vand og danner nye ioner i processen.
Jupiterimages/Photos.com/Getty Images
Trin 1:Identificer reaktanterne
Formlen for ammoniak er NH3 og for vand er den H2O.
Trin 2:Overfør en proton
Fjernelse af en proton (H⁺) fra vand giver hydroxidionen (OH⁻). Tilføjelse af denne proton til ammoniak omdanner den til ammoniumionen (NH₄⁺).
Trin 3:Tildel gebyrer
Protonoverførslen efterlader vand negativt ladet (OH⁻) og ammoniak positivt ladet (NH4⁺). Derfor bærer produkterne disse gebyrer.
Trin 4:Skriv den balancerede ligning
NH3 + H2O → NH4+ + OH⁻
Fordi ligevægtskonstanten for denne basehydrolyse (K_b ≈ 1,8×10⁻⁵) er lille, er reaktionen kun delvist fuldstændig; ammoniak forbliver for det meste udissocieret i fortyndede opløsninger.
For et dybere dyk, se Journal of Chemical Education eller RSC Learning Chemistry side.
 Varme artikler
Varme artikler
-
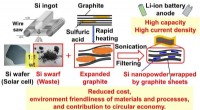 Fra skrald til skat:Siliciumaffald finder ny anvendelse i Li-ion-batterierFig. 1 Fremstilling af elektrode med Si-spåner/grafitpladekompositter (kredit:Osaka University) Li-ion-batterier (LIBer) er meget udbredt i mobilelektronik. Bekymringer for global opvarmning og kl
Fra skrald til skat:Siliciumaffald finder ny anvendelse i Li-ion-batterierFig. 1 Fremstilling af elektrode med Si-spåner/grafitpladekompositter (kredit:Osaka University) Li-ion-batterier (LIBer) er meget udbredt i mobilelektronik. Bekymringer for global opvarmning og kl -
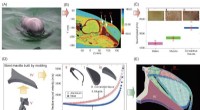 Kunstige materialer rekonstruerer marsvins ekkolokaliseringDesignet af den fysisk baserede fysiske model Kredit:©Science China Press Over millioner af år, Marsvin har udviklet kraftfulde biosonarer med høj nøjagtighed og intelligens til at detektere og sp
Kunstige materialer rekonstruerer marsvins ekkolokaliseringDesignet af den fysisk baserede fysiske model Kredit:©Science China Press Over millioner af år, Marsvin har udviklet kraftfulde biosonarer med høj nøjagtighed og intelligens til at detektere og sp -
 Meget selvlysende blæk fremstillet af kobber-jod hybridklynger med aggregeringsinduceret emissionKredit:Wiley Kinesiske videnskabsmænd har forvandlet kobber-jod-klyngemolekyler til aggregerede, stærkt luminescerende nanostrukturer til brug i lysdioder (LEDer). Faststofsamlingerne lavet af kom
Meget selvlysende blæk fremstillet af kobber-jod hybridklynger med aggregeringsinduceret emissionKredit:Wiley Kinesiske videnskabsmænd har forvandlet kobber-jod-klyngemolekyler til aggregerede, stærkt luminescerende nanostrukturer til brug i lysdioder (LEDer). Faststofsamlingerne lavet af kom -
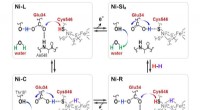 Mikroorganismer bygger de bedste brændstofeffektive brintcellerProtoner overføres mellem det aktive NiFe-sted og det omgivende protein gennem Cyt546- og Glu34-resterne under den katalytiske reaktion af [NiFe]-hydrogenase. Kredit:Shun Hirota For alle de fremsk
Mikroorganismer bygger de bedste brændstofeffektive brintcellerProtoner overføres mellem det aktive NiFe-sted og det omgivende protein gennem Cyt546- og Glu34-resterne under den katalytiske reaktion af [NiFe]-hydrogenase. Kredit:Shun Hirota For alle de fremsk
- De tre hovedtyper af symbiotiske forhold i naturen?
- Hvordan bestemmer solen en skygge?
- Hvad kan P -bølger gøre det
- At være sperm, eller ikke at sperm? Opdagelse af genetisk switch, der bestemmer kønscellernes skæ…
- Har kuldioxid et kogepunkt?
- Undersøgelse kvantificerer elektrontransporteffekterne ved at placere metalkontakter på grafen


