Mestring af kemisk formelskrivning:En praktisk vejledning
Adrian Hernandez/iStock/Getty Images
Brug det periodiske system
At skrive kemiske formler begynder med en solid forståelse af det periodiske system. Tabellen viser alle kendte grundstoffer og parrer dets fulde navn med et kortfattet symbol - H for brint, Cl for klor og så videre. Nogle symboler følger grundstoffets engelske navn (f.eks. O for oxygen), mens andre kommer fra latinske eller græske rødder (Na for natrium, afledt af *natrium*). Når et symbol ikke umiddelbart er tydeligt, er det periodiske system din reference.
Identifikation af kemiske symboler
Inden du udarbejder en formel, skal du identificere hvert atom i forbindelsen eller molekylet. For eksempel er det almindelige bordsalt natriumchlorid; skriv Na for natrium og Cl for chlorid. Den resulterende formel er NaCl. For kovalente forbindelser - dem dannet mellem to ikke-metaller - oversættes navnene ofte direkte til symboler. Præfikser angiver flere atomer:kuldioxid bliver til CO₂, fordi "di‑"-præfikset signalerer to oxygenatomer.
Bestemmelse af valensen
Ioniske forbindelser involverer ladede atomer. Mange periodiske tabeller viser typiske valenser. Gruppe1-metaller er +1-kationer, gruppe2 er +2, og overgangsmetaller (gruppe3-12) kan udvise en række ladninger. Grundstoffer i gruppe 13-18 kan have variable ladninger, mens grupper 15-17 typisk danner anioner med negative ladninger. At kende disse gebyrer er afgørende for at balancere den overordnede formel.
Balancering af gebyrerne
Balancer den samlede ladning for at sikre, at forbindelsen er neutral. For eksempel bærer magnesium (Mg) en ladning på +2, og oxidionen (O²⁻) bærer –2. Kombination af en Mg²⁺ med en O²⁻ giver MgO, en neutral formel. Tilsvarende kræver balancering af magnesiumchlorid to chloridioner (Cl⁻) for hver magnesiumion, hvilket producerer MgCl2.
Skriv den kemiske formel
Nedskrevne angiver antallet af atomer i hvert element. Et enkelt atom er underforstået, så der er ikke skrevet noget "1". I MgO indikerer fraværet af et underskrift et magnesium- og et oxygenatom. Når flere atomer af det samme grundstof er til stede, følger underskriften grundstoffets symbol – MgCl₂ viser to chloratomer pr. magnesium.
Yderligere tips
- Forbindelser, der ender på "‑ide", hører normalt til grupperne 15-17.
- Romertal i parentes, såsom Fe(II), angiver ionens ladning (her +2).
- Polyatomiske ioner (f.eks. hydroxid OH⁻) er grupperet i parentes, når de optræder flere gange:Al(OH)3 er aluminiumhydroxid.
Med regelmæssig praksis vil disse retningslinjer blive en anden natur, hvilket gør dig i stand til at skrive nøjagtige kemiske formler med tillid.
 Varme artikler
Varme artikler
-
 Et kemisk kriterium for bedømmelse af filmSpænding i luften:jo mere nervøse biografgængere er, jo mere isopren de udsender - en målbar indikation af, hvor stressende en film er. Kredit:123RF/Ints Vikmanis Der eksisterer nu et målbart krit
Et kemisk kriterium for bedømmelse af filmSpænding i luften:jo mere nervøse biografgængere er, jo mere isopren de udsender - en målbar indikation af, hvor stressende en film er. Kredit:123RF/Ints Vikmanis Der eksisterer nu et målbart krit -
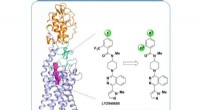 Forskere dechifrerer multi-domænet, struktur i fuld længde af den menneskelige glattede receptorStruktur af multi-domæne human Smoothened receptor, et vigtigt lægemiddelmål for kræftsygdomme. Kredit:ShanghaiTech University Et team af forskere ledet af iHuman Institute of ShanghaiTech Univers
Forskere dechifrerer multi-domænet, struktur i fuld længde af den menneskelige glattede receptorStruktur af multi-domæne human Smoothened receptor, et vigtigt lægemiddelmål for kræftsygdomme. Kredit:ShanghaiTech University Et team af forskere ledet af iHuman Institute of ShanghaiTech Univers -
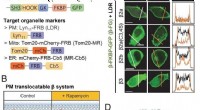 Ny undersøgelse afdækker interaktionen mellem calciumkanalerSubcellulær translokation af CaV β-underenheder ved tilsætning af rapamycin i intakt tsA-201. Kredit:Daegu Gyeongbuk Institut for Videnskab og Teknologi (DGIST) Koreanske forskere har identificere
Ny undersøgelse afdækker interaktionen mellem calciumkanalerSubcellulær translokation af CaV β-underenheder ved tilsætning af rapamycin i intakt tsA-201. Kredit:Daegu Gyeongbuk Institut for Videnskab og Teknologi (DGIST) Koreanske forskere har identificere -
 Ammoniaksyntese - den største innovation i det 20. århundredeTilpasning af de innovationstrin, der er involveret i ammoniaksyntese. Kredit:A. Barona et al./ Sci. Eng. Etik (fotos fra Archiv der Max-Planck-Gesellschaft, Berlin Udover at være et velkendt reng
Ammoniaksyntese - den største innovation i det 20. århundredeTilpasning af de innovationstrin, der er involveret i ammoniaksyntese. Kredit:A. Barona et al./ Sci. Eng. Etik (fotos fra Archiv der Max-Planck-Gesellschaft, Berlin Udover at være et velkendt reng
- Ledtråde til den medfødte lægemiddelresistens af et kakao-fermenterende patogen
- Hvad er et svovl medicin?
- Identificer jordens lag ved deres fysiske?
- Er smeltning af smør fysisk forandring eller kemikalie?
- Kosmiske perler:Fossile muslinger i Florida indeholder beviser for gammel meteorit
- Et nyt beat i kvantestof


