Buten og brom:Forståelse af affarvningsreaktionen
1. Reaktanterne:
* Buten: En alken med en carbon-carbon dobbeltbinding.
* Bromopløsning: Brom (Br₂) opløst i et opløsningsmiddel som dichlormethan eller vand, hvilket giver det en rødbrun farve.
2. Reaktionen:
* Dobbeltbindingen i buten er elektronrig og fungerer som en nukleofil.
* Brommolekylet (Br₂) er polariseret på grund af elektronegativitetsforskellen mellem bromatomer, hvilket gør et bromatom let elektrofilt (elektronelskende).
* Det elektrofile bromatom angriber den elektronrige dobbeltbinding i buten, bryder dobbeltbindingen og danner et bromion-mellemprodukt.
* Det andet bromatom, nu negativt ladet, angriber bromionen fra den modsatte side, hvilket resulterer i dannelsen af en dibromalkan (1,2-dibrombutan).
3. Resultatet:
* Bromopløsningen mister sin rødbrune farve, da bromet forbruges i reaktionen.
* Det farveløse dibromalkanprodukt dannes.
Den overordnede reaktion kan repræsenteres som følger:
CH3CH2CH=CH2 + Br2 → CH3CH2CHBrCH2Br
Nøglepunkter:
* Reaktionen er stereospecifik , hvilket betyder, at produktet er dannet med en specifik stereokemi. I dette tilfælde tilføjes bromatomerne til modsatte sider af dobbeltbindingen, hvilket danner en trans-dibrombutan.
* Denne affarvningsreaktion er en almindelig test for tilstedeværelsen af alkener.
* Reaktionen er også et eksempel på bromering , en specifik type elektrofil addition.
 Varme artikler
Varme artikler
-
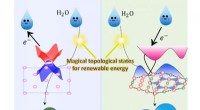 Fremskynde brintproduktionen ved hjælp af de magiske topologiske overfladetilstandeTopologiske ikke-trivielle overfladetilstande kan acceptere eller donere elektroner under vandelektrolyseprocessen. Kredit:MPI CPfS Brintøkonomien anses for at være en af de bedste muligheder fo
Fremskynde brintproduktionen ved hjælp af de magiske topologiske overfladetilstandeTopologiske ikke-trivielle overfladetilstande kan acceptere eller donere elektroner under vandelektrolyseprocessen. Kredit:MPI CPfS Brintøkonomien anses for at være en af de bedste muligheder fo -
 Forskere afslører virkningsmekanisme for lovende kræftforbindelseUNC Linebergers Lee M. Graves, PhD. Kredit:University of North Carolina ved Chapel Hill School of Medicine Forskere fra University of North Carolina Lineberger Comprehensive Cancer Center har afsl
Forskere afslører virkningsmekanisme for lovende kræftforbindelseUNC Linebergers Lee M. Graves, PhD. Kredit:University of North Carolina ved Chapel Hill School of Medicine Forskere fra University of North Carolina Lineberger Comprehensive Cancer Center har afsl -
 Livets kilde:Vanddråber rummer den hemmelige ingrediens til at opbygge livKredit:CC0 Public Domain Purdue University kemikere har afsløret en mekanisme til, at peptiddannende reaktioner kan forekomme i vand - noget, der har undret videnskabsmænd i årtier. Dette er i bun
Livets kilde:Vanddråber rummer den hemmelige ingrediens til at opbygge livKredit:CC0 Public Domain Purdue University kemikere har afsløret en mekanisme til, at peptiddannende reaktioner kan forekomme i vand - noget, der har undret videnskabsmænd i årtier. Dette er i bun -
 Det bedste fra begge verdener:Høj entropi møder lave dimensioner, åbner op for uendelige mulighed…Kredit:Tokyo Tech Opdagelsen af grafen, en 2D lagdelt form af kulstof, engang forårsagede et paradigmeskifte inden for videnskab og teknologi som ingen anden. Da dette vidundermateriale tiltrak
Det bedste fra begge verdener:Høj entropi møder lave dimensioner, åbner op for uendelige mulighed…Kredit:Tokyo Tech Opdagelsen af grafen, en 2D lagdelt form af kulstof, engang forårsagede et paradigmeskifte inden for videnskab og teknologi som ingen anden. Da dette vidundermateriale tiltrak


