Svage syrer:Forståelse af hydrogenionfrigivelse i vandige opløsninger
Her er hvorfor:
* Stærke syrer: Disse syrer ioniseres fuldstændigt (fra hinanden) i vand og frigiver en høj koncentration af H+ ioner. Eksempler omfatter saltsyre (HCl) og svovlsyre (H2SO4).
* Svage syrer: Disse syrer ioniseres kun delvist i vand og frigiver en lav koncentration af H+ ioner. De eksisterer i ligevægt med deres ikke-ioniserede form. Eksempler omfatter eddikesyre (CH3COOH) og kulsyre (H2CO3).
Nøglekarakteristika for svage syrer:
* Lav ioniseringskonstant (Ka): Ka-værdien angiver omfanget af ionisering. Svage syrer har en lille Ka-værdi.
* Lav pH: Mens svage syrer frigiver nogle H+ ioner, har de stadig en lavere pH sammenlignet med stærke syrer.
* Ligevægt: Svage syrer eksisterer i ligevægt med deres konjugerede baser. Det betyder, at de ikke adskilles fuldstændigt til ioner.
Eksempler på svage syrer:
* Eddikesyre (CH3COOH): Findes i eddike.
* Kulsyre (H2CO3): Vigtig til regulering af blodets pH.
* Citronsyre (C6H8O7): Findes i citrusfrugter.
* Flussyre (HF): Anvendes i ætseglas.
Husk, at styrken af en syre bestemmes af dens evne til at donere H+ ioner i opløsning. Svage syrer donerer færre H+ ioner sammenlignet med stærke syrer.
Sidste artikelSvovlsyre:Hvorfor pipetter foretrækkes frem for målecylindre
Næste artikelButen og brom:Forståelse af affarvningsreaktionen
 Varme artikler
Varme artikler
-
 Naturlige fibre trådt ind i satellitter for sikrere missionerKredit:CSIRO En naturlig fiber, der engang indpakkede tidlige egyptiske mumier og blev båret af romerske aristokrater, har fundet et formål i rumalderen. At tråde fibre fra hørplanten gennem satel
Naturlige fibre trådt ind i satellitter for sikrere missionerKredit:CSIRO En naturlig fiber, der engang indpakkede tidlige egyptiske mumier og blev båret af romerske aristokrater, har fundet et formål i rumalderen. At tråde fibre fra hørplanten gennem satel -
 Impulser fra en atomskarp spids gør det muligt for forskere at bryde og danne kemiske bindinger eft…Et internationalt hold af forskere har udviklet en metode til at bryde og danne molekylære bindinger ved at påføre spænding til et molekyle ved hjælp af en skarp spids, der kun er et par atomer bred.
Impulser fra en atomskarp spids gør det muligt for forskere at bryde og danne kemiske bindinger eft…Et internationalt hold af forskere har udviklet en metode til at bryde og danne molekylære bindinger ved at påføre spænding til et molekyle ved hjælp af en skarp spids, der kun er et par atomer bred. -
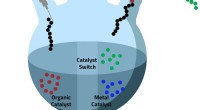 Katalysatorskift betyder, at fire bliver til etVed hjælp af en teknik kaldet katalysatorskift, KAUST -teamet er i stand til at oprette multiblock -polymerer i en enkelt reaktionspotte. © 2019 KAUST Katalysator switch-strategi er nøgletrinnet i
Katalysatorskift betyder, at fire bliver til etVed hjælp af en teknik kaldet katalysatorskift, KAUST -teamet er i stand til at oprette multiblock -polymerer i en enkelt reaktionspotte. © 2019 KAUST Katalysator switch-strategi er nøgletrinnet i -
 Belysning af nanostrukturer i praktiske heterogene katalysatorerNanostrukturen af den heterogene Ziegler-Natta-katalysator blev klarlagt på basis af banebrydende analytiske teknikker. Til venstre:Typiske synkrotrondata og den bestemte nanopartikelmodel af kataly
Belysning af nanostrukturer i praktiske heterogene katalysatorerNanostrukturen af den heterogene Ziegler-Natta-katalysator blev klarlagt på basis af banebrydende analytiske teknikker. Til venstre:Typiske synkrotrondata og den bestemte nanopartikelmodel af kataly


