Beregning af molær masse:En omfattende vejledning
1. Brug af det periodiske system:
* Den mest almindelige metode: Dette er den enkleste og mest pålidelige metode. Du slår atommasserne af hvert grundstof i forbindelsen op på det periodiske system.
* Eksempel: For at finde den molære masse af vand (H₂O), skal du slå atommassen af brint (H) og oxygen (O) op. Derefter ville du lægge dem sammen under hensyntagen til antallet af atomer af hvert element:
* 2 x atommasse af brint (1,008 g/mol) + 1 x atommasse af oxygen (15,999 g/mol) =18,015 g/mol
2. Massespektrometri:
* En kraftfuld analytisk teknik: Denne metode måler direkte masse-til-ladning-forholdet (m/z) af ioner i en prøve.
* Sådan virker det: Prøven ioniseres, og ionerne accelereres gennem et magnetfelt. Ionernes baner påvirkes af deres masse-til-ladning-forhold, hvilket giver mulighed for identifikation og kvantificering af forskellige ioner.
* Applikationer: Massespektrometri bruges på forskellige områder, herunder kemi, biologi og medicin, til at identificere forbindelser, analysere deres sammensætning og bestemme deres molekylvægt.
3. Andre teknikker:
* Titrering: Denne metode kan bruges til at bestemme molmassen af en ukendt syre eller base ved at reagere den med en kendt koncentration af en standardopløsning.
* Kryoskopi og ebullioskopi: Disse teknikker måler ændringer i frysepunktet eller kogepunktet for en opløsning på grund af tilstedeværelsen af et opløst stof. Ændringerne kan bruges til at beregne molmassen af det opløste stof.
Sammenfattende er der ingen enkelt teknik kaldet "Hr. kemi." Molmassen af en kemisk forbindelse bestemmes ved at bruge det periodiske system, massespektrometri eller andre analytiske teknikker som titrering og kryoskopi.
Lad mig vide, hvis du har en bestemt forbindelse, du gerne vil finde molmassen af, så hjælper jeg dig gerne med at beregne den!
 Varme artikler
Varme artikler
-
 Sneeze cam afslører de bedste stofkombinationer til stofmaskerKredit:Pixabay/CC0 Public Domain Under COVID-19-pandemien, Stof ansigtsmasker blev en måde at hjælpe med at beskytte dig selv og andre mod virussen. Og for nogle mennesker, de blev et fashion stat
Sneeze cam afslører de bedste stofkombinationer til stofmaskerKredit:Pixabay/CC0 Public Domain Under COVID-19-pandemien, Stof ansigtsmasker blev en måde at hjælpe med at beskytte dig selv og andre mod virussen. Og for nogle mennesker, de blev et fashion stat -
 Beregning af gennemsnitlig årlig temperatur:En praktisk vejledning til klimaanalyseTilfældigt E. Gartneer Opdateret 24. marts 2022 Guasor/iStock/GettyImages Hvis du har mistanke om, at lokale klimamønstre har ændret sig, giver beregning af den gennemsnitlige årlige temperatur et k
Beregning af gennemsnitlig årlig temperatur:En praktisk vejledning til klimaanalyseTilfældigt E. Gartneer Opdateret 24. marts 2022 Guasor/iStock/GettyImages Hvis du har mistanke om, at lokale klimamønstre har ændret sig, giver beregning af den gennemsnitlige årlige temperatur et k -
 Aluminiumgenbrugsteknologi boostet af krystalliseringsforskningUnder påvirkning af magnetisk omrøring, spiralformede skruelignende krystaller dannes i smeltet legering. Kredit:Dr. Biao Cai En innovativ metode til genanvendelse af aluminium er blevet styrket a
Aluminiumgenbrugsteknologi boostet af krystalliseringsforskningUnder påvirkning af magnetisk omrøring, spiralformede skruelignende krystaller dannes i smeltet legering. Kredit:Dr. Biao Cai En innovativ metode til genanvendelse af aluminium er blevet styrket a -
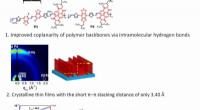 Organisk elektronik:Forskere udvikler en højtydende unipolær n-type tyndfilmstransistorRationelt design af elektrontransporterende organiske halvledende polymerer og deres tyndfilmsanalyse og transistorpræstationer. Kredit: Journal of the American Chemical Society Forskere ved Toky
Organisk elektronik:Forskere udvikler en højtydende unipolær n-type tyndfilmstransistorRationelt design af elektrontransporterende organiske halvledende polymerer og deres tyndfilmsanalyse og transistorpræstationer. Kredit: Journal of the American Chemical Society Forskere ved Toky
- Hvad er to fremskridt med at være multicellulær?
- Methylgrupper og ekstraktion:Forståelse af opløsningsmiddelegenskaber
- Hvad er navnet på denne ioniske forbindelse H3PO4?
- Ny chip-baseret bjælkestyringsanordning lægger grunden til mindre, billigere lidar
- Hvornår fungerede Newton, at tyngdekraften holder solsystemet sammen?
- Er H2NO3 en syre eller en base?


