Ioniseringsenergi og atomstabilitet:et omvendt proportionalt forhold
Her er en oversigt:
* Ioniseringsenergi er den mindste energi, der kræves for at fjerne en elektron fra et gasformigt atom i dets elektroniske jordtilstand.
* Stabilitet henviser til et atoms tendens til at modstå ændringer, såsom at miste elektroner.
Højere ioniseringsenergi betyder et mere stabilt atom:
* Når et atom har en høj ioniseringsenergi, betyder det, at det kræver meget energi at fjerne en elektron. Dette tyder på, at elektronerne er tæt bundet til kernen, hvilket gør atomet mindre tilbøjeligt til at miste en elektron og derfor mere stabilt.
Lavere ioniseringsenergi betyder et mindre stabilt atom:
* Omvendt indikerer en lav ioniseringsenergi, at en elektron let kan fjernes. Dette indebærer, at elektronerne er svagt bundet til kernen, hvilket gør atomet mere tilbøjeligt til at miste en elektron og dermed mindre stabilt.
Nøglefaktorer, der påvirker ioniseringsenergi:
* Atomladning: En højere nuklear ladning (flere protoner) fører til en stærkere tiltrækning mellem kernen og elektronerne, hvilket resulterer i højere ioniseringsenergi og større stabilitet.
* Atomstørrelse: Mindre atomer har elektroner tættere på kernen, oplever en stærkere tiltrækning og har derfor højere ioniseringsenergi og større stabilitet.
* Elektronafskærmning: Elektroner i indre skaller skærmer ydre elektroner fra den fulde nukleare ladning, hvilket reducerer tiltrækningen og sænker ioniseringsenergien, hvilket gør atomet mindre stabilt.
* Elektronkonfiguration: Halvfyldte og fuldt udfyldte underskaller er mere stabile end delvist fyldte. Dette påvirker ioniseringsenergien og dermed stabiliteten.
Eksempel:
* Ædelgasser har meget høje ioniseringsenergier på grund af deres komplette ydre elektronskaller, hvilket gør dem ekstremt stabile.
* Alkalimetaller har meget lav ioniseringsenergi, fordi de kun har én elektron i deres ydre skal, hvilket gør dem let ioniserede og mindre stabile.
Opsummering: Høj ioniseringsenergi indebærer stærk elektron-kerne-tiltrækning, hvilket fører til større stabilitet. Omvendt indebærer lav ioniseringsenergi svag elektron-kerne-tiltrækning, hvilket resulterer i lavere stabilitet.
 Varme artikler
Varme artikler
-
 3D-trykt saltskabelon til bioresorberbare knogleimplantaterHvordan gør man salt og magnesium (venstre) til et knogleimplantat med regelmæssigt strukturerede porer (til højre)? ETH-forskere udviklede en metode ved hjælp af en skabelon med 3D-trykt salt (i midt
3D-trykt saltskabelon til bioresorberbare knogleimplantaterHvordan gør man salt og magnesium (venstre) til et knogleimplantat med regelmæssigt strukturerede porer (til højre)? ETH-forskere udviklede en metode ved hjælp af en skabelon med 3D-trykt salt (i midt -
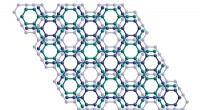 Langhypoteseret næste generations vidundermateriale skabt for første gangKrystalstrukturen af et lag af grafyn. Kredit:Yiming Hu I over et årti har forskere forsøgt at syntetisere en ny form for kulstof kaldet grafyn med begrænset succes. Den bestræbelse er dog nu ved
Langhypoteseret næste generations vidundermateriale skabt for første gangKrystalstrukturen af et lag af grafyn. Kredit:Yiming Hu I over et årti har forskere forsøgt at syntetisere en ny form for kulstof kaldet grafyn med begrænset succes. Den bestræbelse er dog nu ved -
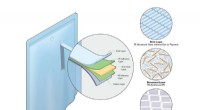 Bygger en bedre polyethylenEmballage, såsom juiceposer, er fremstillet med sammenbundne lag af metal, såsom aluminium, og forskellige typer plast, hvilket gør dem næsten umulige at genbruge. Fordi kun 1-3 procent af sådan embal
Bygger en bedre polyethylenEmballage, såsom juiceposer, er fremstillet med sammenbundne lag af metal, såsom aluminium, og forskellige typer plast, hvilket gør dem næsten umulige at genbruge. Fordi kun 1-3 procent af sådan embal -
 Isbindende molekyler stopper isvækst, fungere som naturligt frostvæskeIs-forspændende simuleringer kan detektere isbindingsstedet for det hyperaktive frostvæskeprotein fra billen Tenebrio molitor, TmAFP. Kredit:Pavithra M. Naullage Visse molekyler binder sig tæt til
Isbindende molekyler stopper isvækst, fungere som naturligt frostvæskeIs-forspændende simuleringer kan detektere isbindingsstedet for det hyperaktive frostvæskeprotein fra billen Tenebrio molitor, TmAFP. Kredit:Pavithra M. Naullage Visse molekyler binder sig tæt til
- Ny forskning baner vejen for simulering af katalysatorer under reaktionsbetingelser
- Hvad er metoderne til bestøvning?
- Er der nogle tips til at skrive redoxreaktioner?
- Hvad er det bedste, hvorfor ved at eliminere methanol fra vand?
- Efter 13 heldige år i Saturn, Cassinis mission er ved at være slut
- Hvordan bidrager mineraler til hårdheden af klipper?


