Svag syredissociation:Forståelse af delvis ionisering
Her er hvorfor:
* Svage syrer er syrer, der kun delvist ioniserer (dissocierer) i opløsning. Det betyder, at de ikke bryder fuldstændigt fra hinanden i deres ioner (H+ og den konjugerede base).
* Stærke syrer , på den anden side, adskilles fuldstændigt i opløsning.
Eksempel:
* Eddikesyre (CH3COOH) er en svag syre. Når det opløses i vand, ioniserer det kun delvist og danner en lille mængde H+ ioner og acetationer (CH3COO-).
* Saltsyre (HCl) er en stærk syre. Det ioniserer fuldstændigt i opløsning og danner en høj koncentration af H+ ioner og chloridioner (Cl-).
Nøgleudtag:
Graden af dissociation af en syre bestemmer dens styrke. Svage syrer dissocierer kun delvist, mens stærke syrer dissocierer fuldstændigt.
 Varme artikler
Varme artikler
-
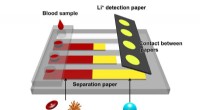 Ny enhed registrerer hurtigt lithiumioner i blod hos patienter med bipolar lidelseDen nyudviklede papirbaserede enhed kan let og billigt måle lithiumionkoncentrationen i blod. Kredit:Komatsu T. et al., ACS -sensorer, 23. april kl. 2020 En gruppe forskere på Hokkaido University
Ny enhed registrerer hurtigt lithiumioner i blod hos patienter med bipolar lidelseDen nyudviklede papirbaserede enhed kan let og billigt måle lithiumionkoncentrationen i blod. Kredit:Komatsu T. et al., ACS -sensorer, 23. april kl. 2020 En gruppe forskere på Hokkaido University -
 Nrl modtager patent på kulstoffangstanordning - et nøgletrin i produktion af syntetisk brændstof …E-CEM (Electrolytic-Cation Exchange Module), udviklet ved US Naval Research Laboratory (NRL), giver flåden mulighed for at producere de råmaterialer, der er nødvendige for at udvikle syntetisk brændst
Nrl modtager patent på kulstoffangstanordning - et nøgletrin i produktion af syntetisk brændstof …E-CEM (Electrolytic-Cation Exchange Module), udviklet ved US Naval Research Laboratory (NRL), giver flåden mulighed for at producere de råmaterialer, der er nødvendige for at udvikle syntetisk brændst -
 Team bruger 3D-print til at optimere gennemstrømningselektroder til elektrokemiske reaktorerFor første gang, Lawrence Livermore National Laboratory-ingeniører har 3D-printede carbonflow-elektroder (FTEer)-porøse elektroder, der er ansvarlige for reaktionerne i reaktorerne-fra grafen-aerogele
Team bruger 3D-print til at optimere gennemstrømningselektroder til elektrokemiske reaktorerFor første gang, Lawrence Livermore National Laboratory-ingeniører har 3D-printede carbonflow-elektroder (FTEer)-porøse elektroder, der er ansvarlige for reaktionerne i reaktorerne-fra grafen-aerogele -
 Effekter af tværbinderlængde på anionbyttermembranbrændselscellerFremskridt inden for brændselscelleteknologi vil hjælpe os kraftigt med at reducere vores brug af fossile brændstoffer til at generere elektricitet, fører til mindre luftforurening. Kredit:Chris LeBou
Effekter af tværbinderlængde på anionbyttermembranbrændselscellerFremskridt inden for brændselscelleteknologi vil hjælpe os kraftigt med at reducere vores brug af fossile brændstoffer til at generere elektricitet, fører til mindre luftforurening. Kredit:Chris LeBou
- Ultrasort tyndfilmsbelægning kunne gøre næste generations teleskoper endnu bedre
- Hvorfor kaldes nitrogen en gas?
- Hvordan tester du, om der er chlorgas?
- COVID-19 har ramt kvinder hårdt, især arbejdende mødre
- Hvordan man bruger entanglement til langdistance- eller frirumkvantekommunikation
- Undersøgelse finder chloroformemissioner, i fremmarch i Østasien, kan forsinke ozonindvindingen me…


