Metaller og saltsyre:Reaktivitet og reaktioner forklaret
* Reaktivitetsserien: Metaller er arrangeret i en reaktivitetsserie, med de mest reaktive øverst.
* Brints position: Brint sidder over mange metaller i denne serie.
* Reaktionsmekanisme: Når et metal reagerer med HCl, mister metalatomerne elektroner og danner positive ioner (kationer). Samtidig får hydrogenioner (H+) fra HCl elektroner til at danne brintgas (H2).
Metaller, der reagerer med fortyndet saltsyre (fra mest til mindst reaktivt):
1. Alkalimetaller (gruppe 1): Lithium (Li), Natrium (Na), Kalium (K), Rubidium (Rb), Cæsium (Cs), Francium (Fr) - Reager kraftigt og producerer brintgas og et metalchlorid.
2. Alkaliske jordmetaller (gruppe 2): Beryllium (Be), Magnesium (Mg), Calcium (Ca), Strontium (Sr), Barium (Ba), Radium (Ra) - Reagerer mindre kraftigt end gruppe 1-metaller og danner brintgas og et metalchlorid.
3. Aluminium (Al): Reagerer langsomt med fortyndet HCl og danner hydrogengas og aluminiumchlorid.
4. Zink (Zn): Reagerer let med fortyndet HCl og danner hydrogengas og zinkchlorid.
5. Jern (Fe): Reagerer med fortyndet HCl og danner hydrogengas og jern(II)chlorid.
6. Tin (Sn): Reagerer langsomt med fortyndet HCl og danner hydrogengas og tin(II)chlorid.
7. Lead (Pb): Reagerer meget langsomt med fortyndet HCl og danner hydrogengas og bly(II)chlorid.
Metaller, der IKKE reagerer med fortyndet saltsyre:
* Metaller under hydrogen i reaktivitetsserien: Kobber (Cu), Sølv (Ag), Guld (Au), Platin (Pt) - Disse metaller er mindre reaktive end brint og vil ikke fortrænge det fra HCl.
Bemærk: Reaktionshastigheden varierer afhængigt af metallets reaktivitet og koncentrationen af syren.
 Varme artikler
Varme artikler
-
 Targeting viral RNA:Grundlaget for næste generations bredspektrede antivirale lægemidlerDette er en computergrafik af et RNA -molekyle. Kredit:Richard Feldmann/Wikipedia En ny tilgang til bekæmpelse af vira ved at målrette mod kontrolcenteret i viralt RNA kan føre til bredspektrede a
Targeting viral RNA:Grundlaget for næste generations bredspektrede antivirale lægemidlerDette er en computergrafik af et RNA -molekyle. Kredit:Richard Feldmann/Wikipedia En ny tilgang til bekæmpelse af vira ved at målrette mod kontrolcenteret i viralt RNA kan føre til bredspektrede a -
 En naturinspireret belægning for at forhindre, at stoffer nedbrydes for tidligtForskere har udviklet en tynd belægning, der kan gøre det muligt for medicin at have færre tilsætningsstoffer. Kredit:Shutterstock.com Kemikere har udviklet en belægning, der kan gøre visse lægemi
En naturinspireret belægning for at forhindre, at stoffer nedbrydes for tidligtForskere har udviklet en tynd belægning, der kan gøre det muligt for medicin at have færre tilsætningsstoffer. Kredit:Shutterstock.com Kemikere har udviklet en belægning, der kan gøre visse lægemi -
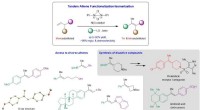 Stereoselektiv alkensyntese med ikke-ædel nikkelkatalyseSkematisk, der viser udviklingen af et nyt Ni-katalyseret system, der konverterer billige og let tilgængelige monosubstituerede olefiner til højværdi tri- og tetrasubstituerede analoger, og dets anv
Stereoselektiv alkensyntese med ikke-ædel nikkelkatalyseSkematisk, der viser udviklingen af et nyt Ni-katalyseret system, der konverterer billige og let tilgængelige monosubstituerede olefiner til højværdi tri- og tetrasubstituerede analoger, og dets anv -
 Undgå bobleproblemer:Undersøgelse af forholdet mellem bobler og elektrokemiFigur 1. Dannelse af bobler på overfladen af en elektrode. Kredit:University of Twente Bobler er kendt for at påvirke energi og masseoverførsel i gasudviklende elektroder. Mange elektrokemiske r
Undgå bobleproblemer:Undersøgelse af forholdet mellem bobler og elektrokemiFigur 1. Dannelse af bobler på overfladen af en elektrode. Kredit:University of Twente Bobler er kendt for at påvirke energi og masseoverførsel i gasudviklende elektroder. Mange elektrokemiske r
- Hvilken energiniveau Shell ville have den største potentielle energi?
- Amerikanske politiske forbud mod forskningsudviklingsproduktion, der lagrer og erhverver biologiske …
- Hvor længe vil solen fortsætte med at skinne?
- Hvad er 160f i Celsius?
- En asteroid på 13 kg rejser med hastighed 110 meter s, når den bryder ind i 3 lige store stykker e…
- Er solen større end Rigel?


