Forståelse af 'Som opløses som':Polaritet og opløselighed i kemi
Like opløses som:Et nærmere kig
Reglen "ligesom opløser ligesom" er et grundlæggende princip i kemi, især i forståelsen af stoffers opløselighed. Det hedder i det væsentlige, at stoffer med lignende polariteter har tendens til at opløses i hinanden.
Polaritet og opløselighed:
* Polaritet refererer til fordelingen af elektrisk ladning i et molekyle. Polære molekyler har en positiv og en negativ ende, hvilket skaber et dipolmoment. Eksempler inkluderer vand (H2O) og ethanol (CH3CH2OH).
* Ikke-polær molekyler har en jævn ladningsfordeling uden tydelige positive eller negative ender. Eksempler omfatter olie og fedt.
Sådan fungerer reglen:
* Polære opløsningsmidler opløse polære opløste stoffer . Dette skyldes, at den positive ende af opløsningsmiddelmolekylet kan interagere med den negative ende af det opløste molekyle og omvendt og danne stærke tiltrækninger.
* Ikke-polære opløsningsmidler opløse ikke-polære opløste stoffer . De kræfter, der holder disse molekyler sammen, er svage Van der Waals-kræfter. Lignende kræfter eksisterer mellem opløsningsmiddel- og opløste molekyler, hvilket tillader dem at blande sig.
Strukturens bidrag:
Strukturen af et molekyle spiller en afgørende rolle for at bestemme dets polaritet og dermed dets opløselighed. Sådan gør du:
* Funktionelle grupper: Forskellige funktionelle grupper i et molekyle bidrager til dets polaritet. For eksempel gør tilstedeværelsen af en hydroxylgruppe (-OH) i ethanol den polær, mens fraværet af sådanne grupper i carbonhydrider gør dem upolære.
* Molekylær form: Formen af et molekyle kan påvirke dets interaktioner med andre molekyler. Lineære molekyler har tendens til at være mere polære end forgrenede molekyler.
* Intermolekylære kræfter: Typen og styrken af intermolekylære kræfter til stede i et molekyle spiller også en rolle i opløseligheden. Polære molekyler har stærkere dipol-dipol-interaktioner, mens ikke-polære molekyler har svagere London-spredningskræfter.
Eksempler:
* Vand (polært opløsningsmiddel) opløser sukker (polært opløst stof), men ikke olie (ikke-polært opløsningsmiddel). De polære vandmolekyler kan danne stærke brintbindinger med de polære sukkermolekyler, hvilket fører til opløsning.
* Olie (ikke-polært opløsningsmiddel) opløser fedt (ikke-polært opløst stof), men ikke salt (polært opløsningsmiddel). De ikke-polære oliemolekyler kan interagere med de ikke-polære fedtmolekyler gennem svage Van der Waals-kræfter.
Undtagelser:
* Amfifile molekyler: Disse molekyler har både polære og ikke-polære områder. For eksempel har sæbemolekyler et polært hoved og en ikke-polær hale. De kan opløse både polære og ikke-polære stoffer.
* Brintbinding: Molekyler, der kan danne brintbindinger (som vand) kan nogle gange opløse molekyler, der ikke er strengt polære, men som stadig kan interagere med vand gennem hydrogenbinding.
Som konklusion:
Reglen "som opløser ligesom" er en hjælpsom vejledning, men det er vigtigt at huske, at det ikke er en hård og hurtig regel. Struktur, intermolekylære kræfter og andre faktorer spiller også en væsentlig rolle ved bestemmelse af opløselighed. Forståelse af disse faktorer giver os mulighed for bedre at forudsige og forklare opløseligheden af forskellige stoffer.
 Varme artikler
Varme artikler
-
 Grønt brint:Nanostruktureret nikkelsilicid skinner som en katalysatorTransmissionselektronmikroskopi (TEM) af den katalytisk aktive fase blev kombineret med energidispersiv røntgenspektroskopi for at kortlægge fordelingen af Ni (grøn), Si (blå) og oxygen (rød) omkrin
Grønt brint:Nanostruktureret nikkelsilicid skinner som en katalysatorTransmissionselektronmikroskopi (TEM) af den katalytisk aktive fase blev kombineret med energidispersiv røntgenspektroskopi for at kortlægge fordelingen af Ni (grøn), Si (blå) og oxygen (rød) omkrin -
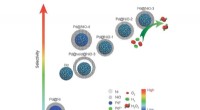 Interface engineering core@shell nanopartikler til aktiv og selektiv direkte H2O2-genereringSkematisk illustration, der viser aktiviteten og selektiviteten over for H2O2-syntese af 5 vægt% Pd@Ni-3/TiO2, 5 vægt% Pd@NiO-x/TiO2 (x =1, 2, 3, 4), 5 vægt% Pd@void@Ni-3/TiO2 og 5 vægt% Pd/Ti02. Kred
Interface engineering core@shell nanopartikler til aktiv og selektiv direkte H2O2-genereringSkematisk illustration, der viser aktiviteten og selektiviteten over for H2O2-syntese af 5 vægt% Pd@Ni-3/TiO2, 5 vægt% Pd@NiO-x/TiO2 (x =1, 2, 3, 4), 5 vægt% Pd@void@Ni-3/TiO2 og 5 vægt% Pd/Ti02. Kred -
 De fem mest mærkelige giftstoffer, der kan dræbe digDer er nogle skøre giftstoffer i vores verden, og de findes ofte i ting, du mindst ville forvente. I denne uges afsnit af Reaktioner, vi nedbryder vores top fem mærkeligste giftstoffer.
De fem mest mærkelige giftstoffer, der kan dræbe digDer er nogle skøre giftstoffer i vores verden, og de findes ofte i ting, du mindst ville forvente. I denne uges afsnit af Reaktioner, vi nedbryder vores top fem mærkeligste giftstoffer. -
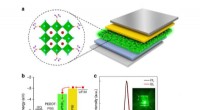 Ny tilgang til forbedring af perovskitfilmers stabilitet og optiske egenskabera) Enhedsstruktur og et tilsvarende tværsnits-TEM-billede af flerlags PeLEDerne; b) Skematisk fladbånds energidiagram over PeLED; c) Normaliseret fotoluminescensspektrum af CsPbBr3 -filmen, og elektro
Ny tilgang til forbedring af perovskitfilmers stabilitet og optiske egenskabera) Enhedsstruktur og et tilsvarende tværsnits-TEM-billede af flerlags PeLEDerne; b) Skematisk fladbånds energidiagram over PeLED; c) Normaliseret fotoluminescensspektrum af CsPbBr3 -filmen, og elektro
- Hvilken betydning har sommersolhverv i forhold til stilling og længste dagår"?
- Undersøgelse undersøger skjulte marketingrelationer på sociale medier
- GPS er ikke kun til vejture længere
- Undersøgelse peger på en proces, der kunne have ført til de første organiske molekyler
- Når du kaster en bold, hvad handler kræfterne på den?
- Hvor mange atomer i 4mgso4?


