Sølvkloridproduktion:Beregning af masse fra nitratopløsning
1. Skriv den afbalancerede kemiske ligning:
Reaktionen mellem sølvnitrat (AgNO₃) og chloridioner (Cl⁻) producerer sølvchlorid (AgCl) som et bundfald:
AgNO3(vandig) + Cl⁻(vandig) → AgCl(s) + NO3⁻(vandig)
2. Beregn antallet af mol sølvnitrat:
Molaritet (M) =mol (mol) / volumen (L)
mol (mol) =Molaritet (M) * volumen (L)
mol AgN03 =0,141 M * 1,85 L =0,26065 mol
3. Bestem den begrænsende reaktant:
Da problemet giver mængden af sølvnitrat, antager vi, at det er den begrænsende reaktant. Det betyder, at mængden af produceret sølvchlorid vil blive bestemt af mængden af tilstedeværende sølvnitrat.
4. Brug molforholdet til at finde mol sølvchlorid:
Fra den afbalancerede ligning producerer 1 mol AgNO3 1 mol AgCl. Derfor:
mol AgCl =mol AgN03 =0,26065 mol
5. Beregn massen af sølvchlorid:
masse (g) =mol (mol) * molær masse (g/mol)
molær masse af AgCl =107,87 g/mol (Ag) + 35,45 g/mol (Cl) =143,32 g/mol
masse AgCl =0,26065 mol * 143,32 g/mol =37,3 g
Derfor kan 37,3 gram sølvchlorid fremstilles ud fra 1,85 L af en 0,141 M sølvnitratopløsning.
 Varme artikler
Varme artikler
-
 Forskere udvikler en diagnostisk test, som har til formål at påvise antibiotikaresistens på mindr…Kredit:Medicinsk Forskningsråd Forskere udvikler en lav pris, hurtig diagnostisk sensortest, som har til formål at vise bakteriers modtagelighed for antibiotika inden for 45 minutter. NHS laborat
Forskere udvikler en diagnostisk test, som har til formål at påvise antibiotikaresistens på mindr…Kredit:Medicinsk Forskningsråd Forskere udvikler en lav pris, hurtig diagnostisk sensortest, som har til formål at vise bakteriers modtagelighed for antibiotika inden for 45 minutter. NHS laborat -
 Ny metode til at bekæmpe kræft med molekylære fibreKræftcellernes fysiske strukturer forstyrres af en bane, der danner indersiden af cellerne - hvilket aktiverer deres selvdestruktionsmekanisme. Kredit:MPI-P Ifølge Tysklands forbundsstatistiske
Ny metode til at bekæmpe kræft med molekylære fibreKræftcellernes fysiske strukturer forstyrres af en bane, der danner indersiden af cellerne - hvilket aktiverer deres selvdestruktionsmekanisme. Kredit:MPI-P Ifølge Tysklands forbundsstatistiske -
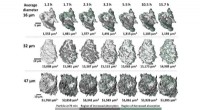 Cementerer fremtidenBilleddannelse af udviklingen af tre cementpartikler. Grøn indikerer opløste mineraler, hulrum og mineralske forbindelser med lav masse. Mørkegrå indikerer solide materialer. Billeddannelsen indiker
Cementerer fremtidenBilleddannelse af udviklingen af tre cementpartikler. Grøn indikerer opløste mineraler, hulrum og mineralske forbindelser med lav masse. Mørkegrå indikerer solide materialer. Billeddannelsen indiker -
 Sådan neutraliseres muriatinsyrespild sikkertKlaus Vedfelt/Getty Images Muriatinsyre, også kendt som saltsyre (HCl), er et almindeligt industri- og husholdningskemikalie. Selv i fortyndet form kan det irritere øjne, hud og luftveje, mens koncen
Sådan neutraliseres muriatinsyrespild sikkertKlaus Vedfelt/Getty Images Muriatinsyre, også kendt som saltsyre (HCl), er et almindeligt industri- og husholdningskemikalie. Selv i fortyndet form kan det irritere øjne, hud og luftveje, mens koncen
- Hvad er opløsningsmiddel og opløsningsmiddel i husholdningsammoniak?
- Hvilken forbindelse indeholder ikke kulstof og brint sammen?
- Hvad er de 4 største planeter i solsystemet?
- Hvad er centigrambalancen for et objekt, der har en masse 2.62114g?
- Hvad er navnet på mikrober, der producerer de fleste antibiotika?
- En centimeter er den samme som hvor mange meter?


