Trigonale plane molekyler og ioner:identifikation og eksempler
Forstå trigonal plan geometri
* Centralatom: Det centrale atom i et trigonalt plant molekyle har tre bindingspar af elektroner og ingen ensomme par.
* Bindningsvinkler: Bindingsvinklerne mellem de tre atomer bundet til det centrale atom er ca. 120°.
* Form: De tre atomer bundet til det centrale atom danner en flad trekant, med det centrale atom i midten.
Eksempler på trigonale plane molekyler og ioner:
* Bortrifluorid (BF₃): Bor har tre valenselektroner, og det danner tre enkeltbindinger med fluoratomer. Dette resulterer i en trigonal plan struktur.
* Culdioxid (CO₂): Kulstof har fire valenselektroner, og det danner to dobbeltbindinger med oxygenatomer. Dobbeltbindingerne behandles som enkeltbindinger med det formål at bestemme formen, så CO₂ har en trigonal plan struktur.
* Nitration (NO₃⁻): Nitrogen har fem valenselektroner. Det danner tre enkeltbindinger med oxygenatomer og har ét ensomt elektronpar. Imidlertid er det enlige par delokaliseret, hvilket betyder, at det er spredt ud over de tre iltatomer, og det påvirker ikke den overordnede form væsentligt. Nitrationen har en trigonal plan struktur.
* Phosphin (PH₃): Fosfor har fem valenselektroner. Den danner tre enkeltbindinger med brintatomer og har ét ensomt elektronpar. Dette enlige par skubber de tre hydrogenatomer ned, hvilket resulterer i en trigonal pyramideformet struktur, ikke trigonal plan.
Nøgleudtag:
For at afgøre, om et molekyle eller en ion har en trigonal plan form, skal du kigge efter et centralt atom med tre bindingspar og ingen ensomme elektronpar.
 Varme artikler
Varme artikler
-
 Forbedring af varmegenanvendelse med termodiffusionseffektenKredit:CC0 Public Domain Absorptionsvarme transformatorer kan effektivt genbruge spildvarmen, der genereres i forskellige industrier. I disse enheder, specialiserede væsker danner tynde film, når
Forbedring af varmegenanvendelse med termodiffusionseffektenKredit:CC0 Public Domain Absorptionsvarme transformatorer kan effektivt genbruge spildvarmen, der genereres i forskellige industrier. I disse enheder, specialiserede væsker danner tynde film, når -
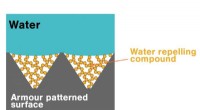 Super vandafvisende materialer er nu holdbare nok til den virkelige verdenEn skematisk fremstilling af, hvordan overfladen ser ud, og hvordan strukturen afviser vand. Kredit:Aalto Universitet Superhydrofobe overflader afviser vand som intet andet. Dette gør dem yderst a
Super vandafvisende materialer er nu holdbare nok til den virkelige verdenEn skematisk fremstilling af, hvordan overfladen ser ud, og hvordan strukturen afviser vand. Kredit:Aalto Universitet Superhydrofobe overflader afviser vand som intet andet. Dette gør dem yderst a -
 At finde kilden til kemiske reaktionerKredit:CC0 Public Domain Forskere søger konstant efter kilden til ting som universets oprindelse, materie eller liv. Forskere ved U.S. Department of Energys (DOE) Argonne National Laboratory, i et
At finde kilden til kemiske reaktionerKredit:CC0 Public Domain Forskere søger konstant efter kilden til ting som universets oprindelse, materie eller liv. Forskere ved U.S. Department of Energys (DOE) Argonne National Laboratory, i et -
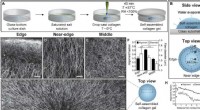 Marangoni-strømme driver justeringen af fibrillære celleladede hydrogelerSelvsamling af kollagen i fordampende dråber genererer afstemte netværk af kollagenfibre. Skematisk af (A) drop-casting procedure og (B) ovenfra og fra siden af en fordampende dråbe kollagen. CRM-bi
Marangoni-strømme driver justeringen af fibrillære celleladede hydrogelerSelvsamling af kollagen i fordampende dråber genererer afstemte netværk af kollagenfibre. Skematisk af (A) drop-casting procedure og (B) ovenfra og fra siden af en fordampende dråbe kollagen. CRM-bi


