Ioniske forbindelser:struktur, dannelse og eksempler
Her er en opdeling:
* Kationer: Disse dannes, når et atom mister en eller flere elektroner, hvilket resulterer i en netto positiv ladning. Eksempler omfatter natrium (Na+) og calcium (Ca2+).
* Anioner: Disse dannes, når et atom får en eller flere elektroner, hvilket resulterer i en netto negativ ladning. Eksempler omfatter chlorid (Cl-) og oxid (O2-).
Disse modsat ladede ioner tiltrækker hinanden og danner en stærk elektrostatisk binding kaldet en ionisk binding . Den resulterende forbindelse er generelt neutral, da de positive og negative ladninger balancerer.
Nøgleegenskaber for ioniske forbindelser:
* Fast ved stuetemperatur: De stærke elektrostatiske kræfter holder ionerne i en stiv, krystallinsk struktur.
* Høje smelte- og kogepunkter: At bryde ionbindingerne kræver meget energi.
* Leder elektricitet, når det er smeltet eller opløst i vand: Frie ioner er i stand til at bevæge sig og føre elektrisk strøm.
* Skørt: Den stive struktur gør dem tilbøjelige til at gå i stykker under stress.
Eksempler på ioniske forbindelser:
* Natriumchlorid (NaCl): Natrium (Na+) kation og chlorid (Cl-) anion.
* Calciumoxid (CaO): Calcium (Ca2+) kation og oxid (O2-) anion.
* Magnesiumsulfat (MgSO4): Magnesium (Mg2+) kation og sulfat (SO42-) anion.
Lad mig vide, hvis du gerne vil vide mere om specifikke ioniske forbindelser eller processen med ionbinding!
Sidste artikelMolekylær kontakt:Definition, typer og betydning i videnskab
Næste artikelAlmindelige syrer:eksempler og deres anvendelser
 Varme artikler
Varme artikler
-
 Defekter på overfladen af katalysatorer bestemmer deres aktivitetModel af et atomart trin på en katalysatoroverflade. På sådanne steder på en koboltkatalysator, den industrielle Fischer-Tropsch-syntese af dieselbrændstof finder sted. Kredit:J. Winterlin/LMU Man
Defekter på overfladen af katalysatorer bestemmer deres aktivitetModel af et atomart trin på en katalysatoroverflade. På sådanne steder på en koboltkatalysator, den industrielle Fischer-Tropsch-syntese af dieselbrændstof finder sted. Kredit:J. Winterlin/LMU Man -
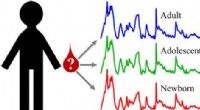 Brug af blodpletter på gerningssteder for at bestemme alderen på en mistænkt eller offerKredit:American Chemical Society Fra sprøjteanalysen gjort berømt i tv -programmet Dexter til den hyppige DNA -profilering af CSI og de reelle sager, der er omfattet af FBI filer , blodprøve
Brug af blodpletter på gerningssteder for at bestemme alderen på en mistænkt eller offerKredit:American Chemical Society Fra sprøjteanalysen gjort berømt i tv -programmet Dexter til den hyppige DNA -profilering af CSI og de reelle sager, der er omfattet af FBI filer , blodprøve -
 En lovende strategi til at øge aktiviteten i antimikrobielle peptiderKredit:Institut national de la recherche scientifique I en artikel offentliggjort for nylig i Plos One , forskere fra INRS-Institut Armand-Frappier Research Center rapporterede en strategi, der
En lovende strategi til at øge aktiviteten i antimikrobielle peptiderKredit:Institut national de la recherche scientifique I en artikel offentliggjort for nylig i Plos One , forskere fra INRS-Institut Armand-Frappier Research Center rapporterede en strategi, der -
 Forskere arbejder på kuldioxidopsamlingssystemerMissouri S&T professor Fateme Rezaei, venstre, og studerende Harshul Thakkar arbejder sammen i Bertelsmeyer Hall om at udvikle teknologi, der hjælper med at holde astronauter sikre mod kuldioxidopbygn
Forskere arbejder på kuldioxidopsamlingssystemerMissouri S&T professor Fateme Rezaei, venstre, og studerende Harshul Thakkar arbejder sammen i Bertelsmeyer Hall om at udvikle teknologi, der hjælper med at holde astronauter sikre mod kuldioxidopbygn
- Hvad er den mad, der bruges i aerob respiration?
- Hvad er flugthastigheden for planeten Jupiter i miles i timen?
- Hvorfor forskere rejser til Jordens centrum?
- Nøgleindikatorer opdaget for klimaændringernes indvirkning på vandforsyningen i Californien
- Forståelse af planters vejrtrækning:Undersøgelse identificerer nøgleproteinsamspillet bag rytmis…
- Europas brændende sommer:et klima-"reality check"?


