Delokaliserede molekylære orbitaler:Forståelse af elektrondeling
Delokaliserede molekylære orbitaler:Deling af kærligheden (af elektroner)
Forestil dig et molekyle som benzen, med dets skiftende enkelt- og dobbeltbindinger. Du tror måske, at elektronerne sidder fast i de specifikke bindinger, ikke? Forkert! I virkeligheden er de meget mere frisindede og strejfer rundt i hele ringen. Det er her delokaliserede molekylære orbitaler komme i spil.
Her er opdelingen:
1. Molekylære orbitaler dannes, når atomare orbitaler fra forskellige atomer kombineres. Dette sker, når atomer binder sammen.
2. Delokaliserede molekylære orbitaler er en speciel type molekylær orbital, hvor elektronerne ikke er begrænset til en specifik binding men i stedet spredt ud over et større område af molekylet.
Tænk på det sådan her:
* Lokaliserede orbitaler: Elektroner er som børn, der leger i deres egne udpegede legeområder (specifikke bindinger).
* Delokaliserede orbitaler: Elektroner er som teenagere, der strejfer frit rundt i hele huset (hele molekylet).
Nøgletræk ved delokaliserede orbitaler:
* Forbedret stabilitet: Delokalisering sænker den overordnede energi af molekylet, hvilket gør det mere stabilt.
* Øget reaktivitet: Delokaliserede elektroner kan lettere deltage i reaktioner, hvilket gør molekylet mere reaktivt på visse måder.
* Unikke egenskaber: Disse orbitaler bidrager til molekylers unikke fysiske og kemiske egenskaber, såsom farve, ledningsevne og magnetisme.
Eksempler på molekyler med delokaliserede orbitaler:
* Benzen: Elektronerne i ringen er delokaliseret, hvilket giver den aromatiske egenskaber.
* Carbonylforbindelser: Carbonylgruppens pi-elektroner er delokaliseret, hvilket gør dem modtagelige for nukleofile angreb.
* Polymerer: Delokalisering spiller en væsentlig rolle i egenskaberne ved ledende polymerer.
Hvorfor er delokaliserede orbitaler vigtige?
De er afgørende for at forstå adfærden af mange molekyler, især dem med:
* Resonansstrukturer: Delokalisering forklarer, hvorfor resonansstrukturer bare er forskellige måder at repræsentere det samme molekyle på.
* Konjugerede systemer: Disse systemer har skiftende enkelt- og dobbeltbindinger, hvilket giver mulighed for elektrondelokalisering og unikke egenskaber.
* Organiske reaktioner: Mange reaktioner involverer bevægelse af elektroner, og delokaliserede orbitaler spiller en nøglerolle i at lette disse processer.
Afslutningsvis er delokaliserede molekylære orbitaler afgørende for at forstå bindingen og reaktiviteten af mange molekyler. De repræsenterer et fascinerende koncept, hvor elektroner ikke er begrænset til specifikke bindinger, men snarere spredt ud, hvilket fører til øget stabilitet og unikke egenskaber.
 Varme artikler
Varme artikler
-
 Forskere tilbyder virksomheder en ny kemi for grønnere polyurethanEn banebrydende formel for vedvarende energi-NREL-forsker Tao Dong (højre) og tidligere praktikant Stephanie Federle (til venstre) undersøger biobaseret, ikke -toksisk polyurethanharpiks, et lovende a
Forskere tilbyder virksomheder en ny kemi for grønnere polyurethanEn banebrydende formel for vedvarende energi-NREL-forsker Tao Dong (højre) og tidligere praktikant Stephanie Federle (til venstre) undersøger biobaseret, ikke -toksisk polyurethanharpiks, et lovende a -
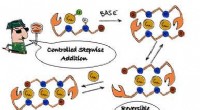 Bygning af molekylære ledninger, et atom ad gangenEn tegneserie af Dr. Rivada-Wheelaghan viser den enkle trinvise proces med kobberatomkædesyntese ved hjælp af en dynamisk ligand. Kobberatomer kan tilføjes eller fjernes en efter en for at lave kæder
Bygning af molekylære ledninger, et atom ad gangenEn tegneserie af Dr. Rivada-Wheelaghan viser den enkle trinvise proces med kobberatomkædesyntese ved hjælp af en dynamisk ligand. Kobberatomer kan tilføjes eller fjernes en efter en for at lave kæder -
 Bakterier kan blive en fremtidig kilde til elektricitetKredit:CC0 Public Domain I de seneste år, forskere har forsøgt at fange den elektriske strøm, som bakterier genererer gennem stofskiftet. Indtil nu, imidlertid, Overførslen af strøm fra bakterie
Bakterier kan blive en fremtidig kilde til elektricitetKredit:CC0 Public Domain I de seneste år, forskere har forsøgt at fange den elektriske strøm, som bakterier genererer gennem stofskiftet. Indtil nu, imidlertid, Overførslen af strøm fra bakterie -
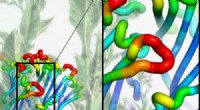 Accelereret opdagelseshastighed kan føre til mere effektive hjælpemidler til rygestopNikotinreceptorer i hjernen er ansvarlige for nikotinafhængighed blandt andre neurologiske roller i CNS. Billedet til venstre viser den komplette receptor, mens det indsatte viser kommunikationsvejen
Accelereret opdagelseshastighed kan føre til mere effektive hjælpemidler til rygestopNikotinreceptorer i hjernen er ansvarlige for nikotinafhængighed blandt andre neurologiske roller i CNS. Billedet til venstre viser den komplette receptor, mens det indsatte viser kommunikationsvejen
- Hvordan kan der ikke oprettes energi?
- Rejser lys som en partikel eller bølge?
- Hvilke fortolkninger af Ayers Rock er givet af evolutionære forskere?
- Hvad er formlen for radioaktivt franciumoxid?
- Roterende film af Pluto og Charon:Det er vist tid
- Hvad er årsagen til at alkoholerne har et højere kogepunkt end alkaner med en lignende molarmasse?…


