Ionisk krystal Ionmobilitet:Forståelse af bevægelse og vibration
* Stærke elektrostatiske kræfter: Ioner i en ionisk krystal holdes sammen af stærke elektrostatiske kræfter mellem modsat ladede ioner. Disse kræfter er stærke nok til at holde ionerne i en fast, stiv gitterstruktur.
* Begrænset bevægelse: Selvom ionerne ikke er frie til at bevæge sig tilfældigt rundt, kan de vibrere i deres positioner inden for krystalgitteret. Denne vibration stiger med temperaturen.
* Konduktivitet: Ioniske forbindelser leder elektricitet når det er smeltet eller opløst i vand. Det skyldes, at ionerne så kan bevæge sig frit og føre en elektrisk strøm. I fast tilstand forhindrer deres begrænsede bevægelse dem i at lede elektricitet.
Nøgleafhentning: Ionerne i ionkrystaller er ikke helt stationære. De kan vibrere, men de kan ikke bevæge sig frit som ioner i en væske.
Sidste artikelForståelse af pH og surhed:Hvordan ændres pH med surhed?
Næste artikelEthansyre og universel indikator:Farveændring forklaret
 Varme artikler
Varme artikler
-
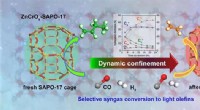 Dynamisk indeslutning af SAPO-17-bure på selektivitetskontrol af syngaskonverteringDynamisk indeslutning af SAPO-17-bure på selektivitetskontrol af syngaskonvertering. Kredit:Wang Haodi og Jiao Feng Et forskerhold ledet af prof. Pan Xiulian og prof. Bao Xinhe fra Dalian Institute
Dynamisk indeslutning af SAPO-17-bure på selektivitetskontrol af syngaskonverteringDynamisk indeslutning af SAPO-17-bure på selektivitetskontrol af syngaskonvertering. Kredit:Wang Haodi og Jiao Feng Et forskerhold ledet af prof. Pan Xiulian og prof. Bao Xinhe fra Dalian Institute -
 I banebrydende metode til at skabe solmateriale, NREL-forskere beviser, at det umulige virkelig ikke…Prøve aluminium III-V solceller, dyrket ved hjælp af HVPE, er vist som Alx(Ga1-x)0.5In0.5P tynde film efter fjernelse af GaAs-substratet bundet til et glashåndtag til transmissionsmålinger. Forskellen
I banebrydende metode til at skabe solmateriale, NREL-forskere beviser, at det umulige virkelig ikke…Prøve aluminium III-V solceller, dyrket ved hjælp af HVPE, er vist som Alx(Ga1-x)0.5In0.5P tynde film efter fjernelse af GaAs-substratet bundet til et glashåndtag til transmissionsmålinger. Forskellen -
 Forskere udvikler semi-flydende metalanode til næste generations batterierCarnegie Mellon-forskere har udviklet en dobbeltledende polymer/carbon-kompositmatrix med lithiummikropartikler, der kan bruges som elektrode i næste generations batterier. Kredit:Carnegie Mellon Univ
Forskere udvikler semi-flydende metalanode til næste generations batterierCarnegie Mellon-forskere har udviklet en dobbeltledende polymer/carbon-kompositmatrix med lithiummikropartikler, der kan bruges som elektrode i næste generations batterier. Kredit:Carnegie Mellon Univ -
 Ny metode til fremstilling af syntetisk DNA3D-model af DNA. Kredit:Michael Ströck/ Wikimedia/ GNU Free Documentation License Kemisk syntetiserede korte DNA-sekvenser er ekstremt vigtige ingredienser med utallige anvendelser i forskningslab
Ny metode til fremstilling af syntetisk DNA3D-model af DNA. Kredit:Michael Ströck/ Wikimedia/ GNU Free Documentation License Kemisk syntetiserede korte DNA-sekvenser er ekstremt vigtige ingredienser med utallige anvendelser i forskningslab
- Ny teknik til kunstig intelligens forbedrer kvaliteten af medicinsk billeddannelse dramatisk
- Nanofibre fjerner vand for farlige farvestoffer:Forskere udvikler effektive filtre baseret på cellu…
- Ionisk ledningsevne i løsninger:Forståelse af mekanismen
- Hvordan dannede der en alpin tundra?
- Polyamider fra terpener:Amorf Caramid-R og semi-krystallinsk Caramid-S
- Neutrale atomer af det samme element kan variere i deres nummer Hvad?


