Borreaktivitet:Forståelse af dens kemiske adfærd
* Høj ioniseringsenergi: Bor har en høj ioniseringsenergi, hvilket betyder, at det kræver meget energi at fjerne en elektron. Dette gør det vanskeligt for bor at danne positive ioner og deltage i ionbinding.
* Stærke kovalente bindinger: Bor danner primært kovalente bindinger, som er stærke og stabile. Det danner ikke let ioniske forbindelser.
* Beskyttende oxidlag: Bor reagerer let med oxygen og danner et beskyttende oxidlag (B2 O3 ). Dette lag fungerer som en barriere, der forhindrer yderligere reaktioner med andre elementer.
Bor kan dog stadig reagere under visse betingelser:
* Høje temperaturer: Bor bliver mere reaktivt ved høje temperaturer. Det kan reagere med halogener, nitrogen og kulstof ved forhøjede temperaturer.
* Stærke oxidationsmidler: Bor kan reagere med stærke oxidationsmidler som salpetersyre og koncentreret svovlsyre.
* Specifikke kemiske reaktioner: Bor kan deltage i specifikke reaktioner, såsom reduktion af metaloxider til dannelse af borider.
Opsummeret er bor generelt ikke-reaktivt under standardbetingelser på grund af dets høje ioniseringsenergi, stærke kovalente bindinger og beskyttende oxidlag. Det kan dog reagere under specifikke forhold, især ved høje temperaturer eller med stærke oxidationsmidler.
 Varme artikler
Varme artikler
-
 Hvordan en vietnamesisk rå svinekødssnack kunne hjælpe os med at holde maden frisk, naturligtVietnamesisk fermenteret svinekødssnack, Nem Chua. Kredit:RMIT University En traditionel vietnamesisk kødsnack kunne indeholde nøglen til at udvikle et sikkert og naturligt fødevarekonserveringsmi
Hvordan en vietnamesisk rå svinekødssnack kunne hjælpe os med at holde maden frisk, naturligtVietnamesisk fermenteret svinekødssnack, Nem Chua. Kredit:RMIT University En traditionel vietnamesisk kødsnack kunne indeholde nøglen til at udvikle et sikkert og naturligt fødevarekonserveringsmi -
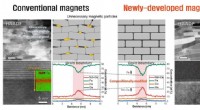 Udvikling af ny magnet, der reducerer brugen af sjældne jordarters grundstoffer med 30 %HAADF-STEM billeder og skematiske illustrationer af konventionelle magneter og nyudviklede magneter. Kredit:Korea Institute of Materials Science (KIMS) Et forskerhold ledet af Dr. Jung-Goo Lee og D
Udvikling af ny magnet, der reducerer brugen af sjældne jordarters grundstoffer med 30 %HAADF-STEM billeder og skematiske illustrationer af konventionelle magneter og nyudviklede magneter. Kredit:Korea Institute of Materials Science (KIMS) Et forskerhold ledet af Dr. Jung-Goo Lee og D -
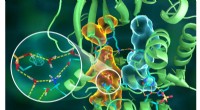 Neutroner maler atomportræt af prototypisk cellesignalingsenzymIllustration af den indviklede organisering af PKA -strukturen, hvor forskellige dele af proteinet er forbundet via udførlige hydrogenbindingsnetværk (stiplede gule linjer), limet sammen af de hydro
Neutroner maler atomportræt af prototypisk cellesignalingsenzymIllustration af den indviklede organisering af PKA -strukturen, hvor forskellige dele af proteinet er forbundet via udførlige hydrogenbindingsnetværk (stiplede gule linjer), limet sammen af de hydro -
 SA36 vs A36 Steel:Nøgleforskelle og applikationerAf Brock Cooper Opdateret 30. august 2022 American Society for Testing and Materials (ASTM) og American Society for Civil Engineers (ASME) udgiver hver især stålstandarder, der ofte ligner hinanden,
SA36 vs A36 Steel:Nøgleforskelle og applikationerAf Brock Cooper Opdateret 30. august 2022 American Society for Testing and Materials (ASTM) og American Society for Civil Engineers (ASME) udgiver hver især stålstandarder, der ofte ligner hinanden,
- Hvad er opbygningen af et planteorgansystem?
- Hvorfor er hypotesen så vigtig for den videnskabelige metode?
- Hvilket element har en emissionslinje ved 768 nm?
- Smarte nanogeler ved luft/vand-grænsefladen:strukturelle undersøgelser af neutronreflektivitet
- Kan du vende biologiuret?
- Undersøgelse afslører ny mekanisme til at forklare, hvordan kontinenter stabiliserede sig


